С.В. Крылов1,2, И.Н. Пасечник2, С.С. Гужев1,2, А.К. Орлецкий1, А.А. Шумский1, Г. Дгебуадзе1, А.Д. Герасенкова1
1ФГБУ «Национальный медицинский исследовательский центр травматологии и ортопедии имени Н.Н. Приорова» Минздрава России, Москва
2ФГБУ ДПО «Центральная государственная медицинская академия» Управления делами Президента Российской Федерации, Москва
РЕЗЮМЕ
Введение. В представленном исследовании изучили влияние блокады подвздошной фасции у пациентов после первичного тотального эндопротезирования тазобедренного сустава (ТЭТС).
Цель работы. Оценка эффективности и безопасности использования блокады подвздошной фасции в послеоперационном периоде после ТЭТС.
Материалы и методы. В исследование включили 60 пациентов, которым выполнили первичное ТЭТС. Пациенты были разделены случайным образом на две группы: группа 1 (n = 30) – пациенты, которым в послеоперационном периоде проводили мультимодальную схему послеоперационной анальгезии; группа 2 (n = 30) – пациенты, которым, кроме мультимодальной анальгезии, выполняли блокаду подвздошной фасции бедра под ультразвуковой навигацией после операции. В послеоперационном периоде регистрировали уровень болевого синдрома в покое и при движении, используя визуально-аналоговую шкалу уровня боли (ВАШ1 и ВАШ2) через 6 –12 –24 –48 часов. Также регистрировали кратность и количество назначения наркотических анальгетиков и отмечали частоту развития побочных эффектов от их использования.
Результаты. Показатели уровня болевого синдрома в покое и при движении в первые 24 часа были ниже у пациентов второй группы. Через 48 часов достоверных различий между группами по уровню боли не обнаружено. Пациентам первой группы чаще назначались опиоидные анальгетики, чем пациентам второй. Количество побочных эффектов от использования наркотических анальгетиков было больше у пациентов первой группы.
Выводы. Использование блокады подвздошной фасции является эффективным методом периоперационной анальгезии после эндопротезирования тазобедренного сустава. Данный метод позволяет достигать высокий уровень обезболивания и снижает потребность в назначении опиоидных анальгетиков.
КЛЮЧЕВЫЕ СЛОВА: регионарная анестезия, блокада периферических нервов, блокада подвздошной фасции, эндопротезирование тазобедренного сустава.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы заявляют об отсутствии конфликта интересов.
Efficiency of fascia iliaca block in total hip arthroplasty
S.V. Krylov1,2, I.N. Pasechnik2, S.S. Guzhev1,2, A.K. Orletskiy1, A.A. Shumskiy1, G. Dgebuadze1, A.D. Gerasenkova1
1National Medical Research Center for Traumatology and Orthopedics n.a. N.N. Priorov, Moscow, Russia
2Central State Medical Academy, Moscow, Russia
SUMMARY
Introduction. The present study examined the effect of iliac fascia blockade in patients after primary total hip arthroplasty (TEH).
Purpose. Evaluation of the efficacy and safety of using the iliac fascia blockade in the postoperative period after TEH.
Materials and methods. The study included 60 patients who underwent primary TEH. Patients were randomly divided into two groups: group 1 (n = 30) – patients who underwent a multimodal scheme of postoperative analgesia in the postoperative period; group 2 (n = 30) – patients who, in addition to multimodal analgesia, underwent blockade of the iliac fascia of the thigh under ultrasound navigation after surgery. In the postoperative period, the level of pain syndrome at rest and during movement was recorded using a visual analog scale of the pain level (VAS1 and VAS2) after 6–12–24–48 hours. We also recorded the frequency and quantity of prescription of narcotic analgesics and noted the frequency of side effects from their use.
Results. The level of pain syndrome at rest and during movement in the first 24 hours was lower in patients of the 2nd group. After 48 hours, there were no significant differences between the groups in the level of pain. Patients in group 1 were prescribed opioid analgesics more often than patients in group 2. The number of side effects from the use of narcotic analgesics was greater in patients of group 1.
Conclusions. The use of the iliac fascia block is an effective method of perioperative analgesia after hip arthroplasty. This method allows achieving a high level of pain relief and reduces the need for prescription of opioid analgesics.
KEYWORDS: regional anesthesia, peripheral nerve block, iliac fascia block, hip arthroplasty.
CONFLICT OF INTEREST. The authors declare no conflict of interest.
Введение
В последние десятилетия во всем мире активно развивается ортопедия крупных суставов. Тотальное эндопротезирование тазобедренного сустава (ТЭТС) является методом выбора в лечении прогрессирующего остеоартрита и остеоартроза [1, 2, 3, 4].
Количество выполняемых операций на тазобедренном суставе ежегодно увеличивается. Это связано как с расширением показаний для выполнения операции с целью восстановления функциональных возможностей, так и совершенствованием хирургической помощи и реабилитации. ТЭТС на сегодняшний момент является наиболее распространенной реконструктивной операцией на тазобедренном суставе и одной из самых распространенных ортопедических операций во всем мире [5, 6].
Одним из наиболее важных моментов в травматологии и ортопедии в целом, и при операциях на тазобедренном суставе в частности, остается адекватное периоперационное обезболивание. Основными задачами являются снижение количества назначений опиоидных анальгетиков и профилактика осложнений, связанных с их использованием. Ранняя реабилитация и активизация пациентов после операции в совокупности с адекватным обезболиванием являются фактором благоприятного течения периоперационного периода и исхода лечения [7, 8].
Использование регионарной анестезии на сегодняшний момент является неотъемлемой частью мультимодального подхода к обезболиванию, позволяющей контролировать уровень болевого синдрома и реализовывать программу ускоренного восстановления и реабилитации в травматологии и ортопедии [9, 10, 11, 12].
Несмотря на большое количество исследований, оптимальный метод регионарной анальгезии в послеоперационном периоде после ТЭТС до сих пор окончательно не определен. Также отсутствуют рекомендации по периоперационной регионарной анальгезии для данных операций [13].
Блокада подвздошной фасции (Fascia iliaca block) является фасциально-футлярной блокадой, которая может быть использована в схеме мультимодальной анальгезии в послеоперационном периоде после ТЭТС. Представленный метод хорошо описан с технической точки зрения, однако эффективность его остается дискутабельной [14, 15, 16].
Целью данного исследования являлась оценка эффективности и безопасности использования БПФ в послеоперационном периоде после ТЭТС.
Материалы и методы
Данное исследование было одобрено локальным этическим комитетом, пациенты были информированы о целях и задачах данной работы, было подписано согласие на участие. В одноцентровое проспективное рандомизированное исследование было включено 60 пациентов, которым планировалось выполнить первичное ТЭТС.
Критерии включения в исследование: согласие пациента на участие в исследовании, отсутствие противопоказаний к регионарной анестезии, способность к сотрудничеству на всех этапах исследования. Критерии исключения из исследования: отказ пациента, отказ от регионарной анестезии, наличие коагулопатии, диагностированный хронический болевой синдром, выраженная энцефалопатия.
Пациенты, отвечающие критериям включения, были рандомизированы «методом конвертов» на две клинические группы: группа 1 (n = 30) – пациенты, которым в послеоперационном периоде проводили мультимодальную схему послеоперационной анальгезии; группа 2 (n = 30) – пациенты, которым кроме мультимодальной анальгезии выполняли блокаду подвздошной фасции бедра под ультразвуковой навигацией после операции.
Протокол предоперационного и интраоперационного периода был одинаковым у пациентов двух групп. В операционной осуществлялся стандартный анестезиологический мониторинг, включающий регистрацию частоты сердечных сокращений, электрокардиографию, неинвазивное измерение артериального давления, насыщение крови кислородом, термометрию. После инфузии 500 мл солевого раствора выполнялась спинномозговая анестезия на уровне L3–L4. Всем пациентам интратекально вводили 15 мг изобарического раствора бупивакаина. После окончания операции, при отсутствии показаний для продолженного динамического наблюдения, пациенты первой группы переводились в профильное отделение, пациентам второй группы выполнялась регионарная блокада согласно дизайну исследования, после чего они также транспортировались в отделение.
Выполнение блокады подвздошной фасции пациентам второй группы
Блокада выполнялась во всех случаях одним анестезиологом-реаниматологом, чтобы избежать возможные технические нюансы ее выполнения. Линейный ультразвуковой датчик с частотой 15 МГц устанавливался на уровень паховой складки для визуализации бедренной артерии и вены, бедренного нерва (рис. 1).
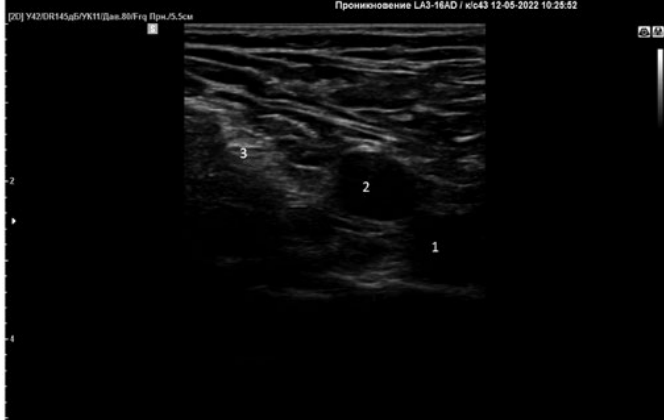
Рисунок 1. Сосудисто-нервный пучок на уровне паховой складки.
Примечание: 1 – бедренная вена, 2 – бедренная артерия, 3 – бедренный нерв).
После этого датчик перемещали в латеральном направлении вдоль подвздошно-поясничной мышцы до визуализации двух листков фасции и подвздошно-поясничной мышцы (рис. 2).
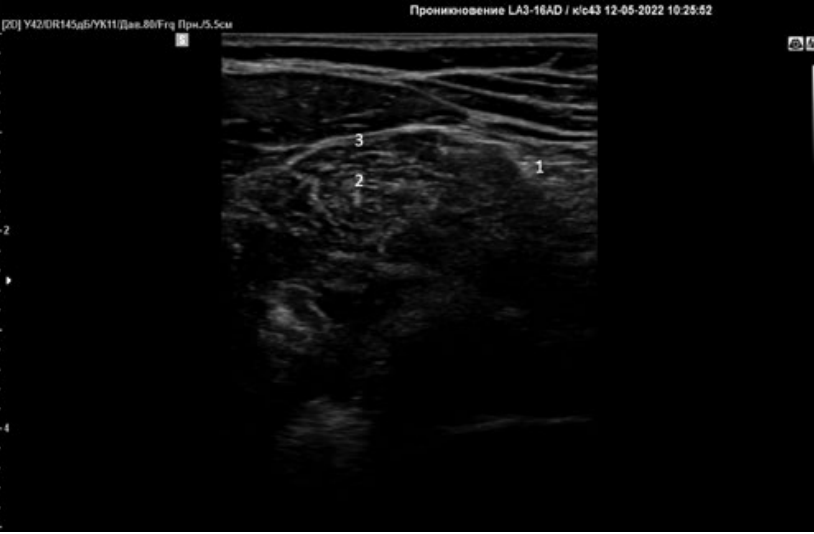
Рисунок 2. Подвздошная фасция.
Примечание: 1 – бедренный нерв, 2 – подвздошно-поясничная мышца, 3 – подвздошная фасция.
Затем игла для проводниковой анестезии подводилась в пространство между подвздошной фасцией и подвздошно-поясничной мышцей. Правильное положение иглы проверяли тестовым введением 1–2 мл раствора местного анестетика. После того как было подтверждено корректное положение иглы, осуществлялось введение местного анестетика под подвздошную фасцию (рис. 3). В качестве местного анестетика в исследовании использовали ропивакаин 0,5% (Рапинов, Россия) – 20 мл.
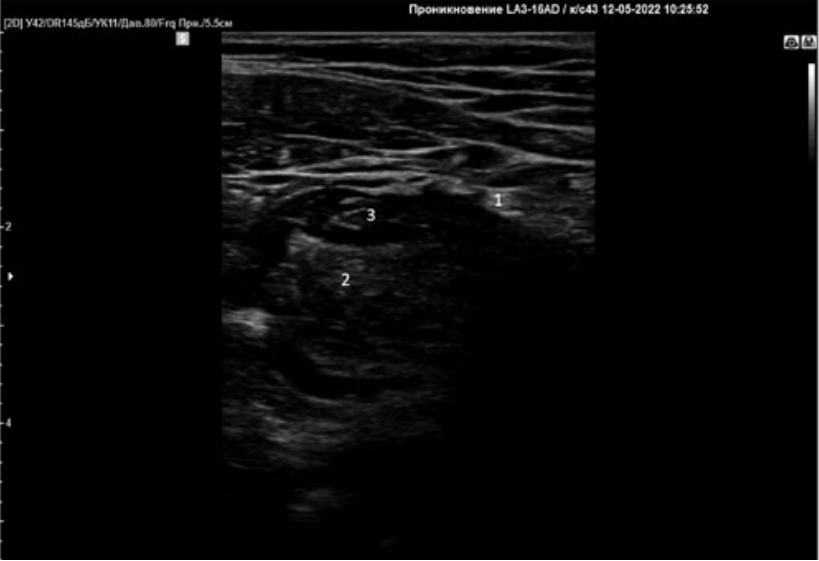
Рисунок 3. Блокада подвздошной фасции.
Примечание: 1 – бедренный нерв, 2 –подвздошно-поясничная мышца, 3 – местный анестетик, введенный под подвздошную фасцию.
В послеоперационном периоде регистрировали уровень болевого синдрома в покое и при движении, используя визуально-аналоговую шкалу уровня боли (ВАШ1 и ВАШ2) через 6 –12 –24 –48 часов. Также регистрировали кратность и количество назначения наркотических анальгетиков и отмечали частоту развития побочных эффектов от их использования.
Всем пациентам назначалась стандартная схема мультимодальной анальгезии в послеоперационном периоде, включающая назначение ацетаминофена 1 г (Ифимол, Индия) 3 раза в день в комбинации с кеторолаком 30 мг (Кеторолак, Россия) 3 раза в день. При наличии выраженного болевого синдрома (болевой синдром, оцениваемый по ВАШ более 3 баллов в покое и 4 баллов при движении) назначались наркотические анальгетики – тримеперидин 2% (Промедол, Россия) – 1 мл.
Статистическая обработка данных
Результаты представлены в виде среднего значения и стандартного отклонений. Нормальность распределения полученных данных оценивали с помощью критерия Шапиро – Уилка. Сравнение между группами осуществляли с использованием t-критерия Стьюдента для независимых переменных. Статистической значимостью в исследовании считали значение p < 0,05. Для расчетов использовалось статистическую программу Statistica 8.
Результаты
Результаты оценки уровня боли в покое и при движении представлены в таблицах 1 и 2.
Таблица 1
Показатели уровня боли в покое (ВАШ1)
| Группа 1 | Группа 2 | |
| 6 часов | 2,4 ± 0,4 | 0,9 ± 0,3* |
| 12 часов | 2,8 ± 0,5 | 1,4 ± 0,3* |
| 24 часа | 2,7 ± 0,6 | 1,6 ± 0,4* |
| 48 часов | 2,5 ± 0,4 | 2,2 ± 0,5 |
Примечание: * – p < 0,05.
Таблица 2
Показатели боли при движении (ВАШ2)
| Группа 1 | Группа 2 | |
| 6 часов | 3,5 ± 0,4 | 1,3 ± 0,3* |
| 12 часов | 3,4 ± 0,6 | 1,6 ± 0,5* |
| 24 часа | 3,8 ± 0,4 | 2,3 ± 0,3* |
| 48 часов | 3,1 ± 0,5 | 3 ± 0,6 |
Примечание: * – p < 0,05.
В результате оценки уровня боли в покое и при движении отмечены достоверно более низкие показатели у пациентов второй группы по сравнению с пациентами первой группы через 6, 12, 24 часа после операции (p < 0,05). Через 48 часов статистически значимых различий в уровне статической и динамической боли не выявлено (p > 0,05).
Количество и кратность назначения опиоидных анальгетиков в послеоперационном периоде продемонстрирована в таблице 3.
Таблица 3
Количество и кратность назначения опиоидных анальгетиков в послеоперационном периоде
| Группа 1 | Группа 2 | |
| Тримеперидин 2%, мг | 50 ± 0,4 | 28 ± 0,3* |
| Кратность назначения, раз | 2,5 ± 0,4 | 1,4 ± 0,3* |
Примечание: * – p < 0,05.
При анализе данных о количестве и кратности назначения наркотических анальгетиков доказано, что пациентам второй группы данные препараты назначались реже и суммарное количество было достоверно меньше в сравнении с пациентами первой группы (p < 0,05).
Побочные эффекты от использования опиоидных анальгетиков в исследуемых группах отражены в таблице 4.
Таблица 4
Побочные эффекты от использования опиоидных анальгетиков
| Группа 1, n = 30 | Группа 2, n = 30 | |
| Кожный зуд, n (%) | 3 (10,0%) | 1 (3,3%) |
| Тошнота, n (%) | 3 (10,0%) | 1 (3,3%) |
| Рвота, n (%) | 2 (6,7%) | – |
| Сонливость, n (%) | 3 (10,0%) | 1 (3,3%) |
| Всего, n (%) | 11 (36,7%) | 4 (9,9%) |
В нашем исследовании было обнаружено большее количество регистрируемых побочных эффектов от назначения наркотических анальгетиков у пациентов первой группы в сравнении с пациентами второй (группа 1 – 36,7%, группа 2 – 9,9%).
Обсуждение
Несмотря на то что с момента описания блокады подвздошной фасции (БПФ) прошло более 10 лет [15], данные о ее эффективности при эндопротезировании тазобедренного сустава до сих пор немногочисленны. Кроме того, большинство имеющихся исследований касаются в основном пациентов с острой травмой, у которых применение БПФ снижает интенсивность болевого синдрома и потребность в наркотических анальгетиках [17, 18, 19].
В некоторых исследованиях у пациентов, которым планировалось выполнение эндопротезирования тазобедренного сустава, было продемонстрировано, что БПФ снижает потребность в послеоперационном назначении опиоидных анальгетиков [20, 21].
В представленном исследовании доказана эффективность использования БПФ в вопросе контроля уровня после эндопротезирования тазобедренного сустава. Болевой синдром в покое и при движении был достоверно ниже у пациентов с БПФ в первые сутки исследования, чем у пациентов с мультимодальной схемой обезболивания.
Не вызывает сомнения тот факт, что использование опиоидных анальгетиков является бесспорным достижением в анестезиологии и реаниматологии для послеоперационного обезболивания, однако количество регистрируемых побочных эффектов от их применения имеет тенденцию к увеличению. В последние десятилетия, помимо таких осложнений, как угнетение дыхания, брадикардия, гипотензия, тошнота и рвота, остро встает вопрос развития опиоидной зависимость или опиоид-индуцированной гипералгезии [22, 23]. Поиск и использование опиоид-сберегающих методов в периоперационном периоде является краеугольным камнем обеспечения безопасности пациента.
Наше исследование продемонстрировало более высокие значения общего количества и кратности назначения опиоидных анальгетиков у пациентов первой группы в сравнении с пациентами второй. Данные результаты сопоставимы с метаанализом Liu et al. и Gao et al., где было доказано, что БПФ снижает потребность в использовании наркотических анальгетиков и интенсивность боли у пациентов, перенесших эндопротезирование тазобедренного сустава [17, 24].
Возникновение послеоперационной тошноты и рвоты, кожного зуда, сонливости наиболее часто встречалось у пациентов первой группы ввиду достоверно большей потребности и количества назначений опиоидных анальгетиков. Данные исследований X.Y. Zhang и Gao Yun et al., которые включали 372 и 325 пациентов после эндопротезирования тазобедренного сустава, показали схожие результаты в частоте возникновения побочных эффектов, вызванных применением опиоидных анальгетиков в послеоперационном периоде [24, 25].
Выводы
Использование БПФ является эффективным методом периоперационной анальгезии после эндопротезирования тазобедренного сустава. Данный метод позволяет достигать высокого уровня обезболивания и снижает потребность в назначении опиоидных анальгетиков. Как следствие этого, снижается риск развития осложнений от их применения. Благоприятное течение раннего послеоперационного периода и отсутствие осложнений, вероятнее всего, приводит к снижению продолжительности пребывания пациента в стационаре, что, безусловно, имеет экономическую эффективность. Результаты, полученные в данном исследовании, дают возможность рекомендовать использование БПФ в вопросе контроля уровня боли и профилактики развития осложнений в периоперационном периоде после эндопротезирования тазобедренного сустава.
Список литературы / References
- Learmonth I.D., Young C., Rorabeck C. The operation of the century: Total hip replacement. Lancet. 2007; 370: 1508–1519. DOI: 10.1016/S0140-6736(07)60457-7.
- National Institutes of Health NIH consensus conference: Total hip replacement. NIH consensus development panel on total hip replacement. JAMA. 1995; 273: 1950–1956. DOI: 10.1001/jama.273.24.1950.
- Kane R.L., Saleh K.J., Wilt T.J., Bershadsky B., Cross W.W., MacDonald R.M., Rutks I. Total knee replacement. Evid. Rep. Technol. Assess. 2003; 86: 1–8.
- Laupacis A., Bourne R., Rorabeck C., Feeny D., Wong C., Tugwell P., Leslie K., Bullas R. The effect of elective total hip replacement on health-related quality of life. J. Bone Jt. Surg. 1993; 75: 1619–1626. DOI: 10.2106/00004623-199311000-00006.
- Felson D.T. The epidemiology of knee osteoarthritis: Results from the Framingham Osteoarthritis Study. Semin. Arthritis Rheum. 1990; 20: 42–50. DOI: 10.1016/0049-0172(90)90046-I.
- Mamlin L.A., Melfi C.A., Parchman M.L., Michael L., Benjamin G., Deborah I., Barry P.K., Robert S.D., David A.H., Deborah A., et al. Management of osteoarthritis of the knee by primary care physicians. Arch. Fam. Med. 1998; 7: 563–567. DOI: 10.1001/archfami.7.6.563.
- Kopp S.L., Børglum J., Buvanendran A. More anesthesia and analgesia practice pathway options for total knee arthroplasty: An evidence-based review by the American and European societies of regional anesthesia and pain medicine. Reg. Anesth. Pain Med. 2017; 42: 683–697. DOI: 10.1097/AAP.0000000000000673.
- Memtsoudis S.G., Sun X., Chiu Y.L., Stundner O., Spencer S.L., Banerjee S., Mazumdar M., Nigel E. Perioperative comparative effectiveness of anesthetic technique in orthopedic patients. Anesthesiology. 2013; 118: 1046–1058. DOI: 10.1097/ALN.0b013e318286061d.
- Misiołek H., Zajączkowska R., Daszkiewicz A., Woroń J., Dobrogowski J., Wordliczek J., Owczuk R. Postoperative pain management – 2018 consensus statement of the section of regional anaesthesia and pain therapy of the polish society of anaesthesiology and intensive therapy, the polish society of regional anaesthesia and pain therapy, the polish association for the study of pain and the national consultant in anaesthesiology and intensive therapy. Anaesthesiol. Intensive Ther. 2018; 50: 173–179.
- Opperer M., Danninger T., Stundner O., Memtsoudis S.G. Perioperative outcomes and type of anesthesia in hip surgical patients: An evidence-based review. World J. Orthop. 2014; 5: 336–343. DOI: 10.5312/wjo.v5.i3.336.
- Husted H., Hansen H.C., Holm G., Bach-Dal C., Rud K., Lande Andersen K., Kehlet H. What determines length of stay after total hip and knee arthroplasty? A nationwide study in Denmark. Arch. Orthop. Trauma Surg. 2010; 130: 263–268. DOI: 10.1007/s00402-009-0940-7.
- Kerr D.R., Kohan L. Local infiltration analgesia: A technique for the control of acute postoperative pain following knee and hip surgery: A case study of 325 patients. Acta Orthop. 2008; 79: 174–183. DOI: 10.1080/17453670710014950.
- Steenberg J., Moller A.M. Systematic review of the effects of fascia iliaca compartment block on hip fracture patients before operation. Br. J. Anaesth. 2018; 120: 1368–1380. DOI: 10.1016/j.bja.2017.12.042.
- Vaughan B., Manley M., Stewart D., Iyer V. Distal injection site may explain lack of analgesia from fascia iliaca block for total hip. Reg. Anesth. Pain Med. 2013; 38: 556–557. DOI: 10.1097/AAP.0000000000000011.
- Hebbard P., Ivanusic J., Sha S. Ultrasound-guided supra-inguinal fascia iliaca block: A cadaveric evaluation of a novel approach. Anaesthesia. 2011; 66: 300–305. DOI: 10.1111/j.1365-2044.2011.06628.x.
- Swenson J.D., Davis J.J., Stream J.O., Crim J.R., Burks R.T., Greis P.E. Local anesthetic injection deep to the fascia iliaca at the level of the inguinal ligament: The pattern of distribution and effects on the obturator nerve. J. Clin. Anesth. 2015; 27: 62–67. DOI: 10.1016/j.jclinane.2015.07.001.
- Liu S.S., Buvanendran A., Rathmell J.P., Sawhney M., James J.B., Moric M., Stephen P., Ashley J.P., Lazaros P., Craig J.D.V., et al. Predictors for moderate to severe acute postoperative pain after total hip and knee replacement. Int. Orthop. 2012; 36: 2261–2267. DOI: 10.1007/s00264-012-1623-5.
- Hong H.K., Ma Y. The efficacy of fascia iliaca compartment block for pain control after hip fracture: A meta-analysis. Medicine. 2019; 98: e16157. DOI: 10.1097/MD.0000000000016157.
- Haines L., Dickman E., Ayvazyan S., Pearl M., Wu S., Rosenblum D., Likourezos A. Ultrasound-guided fascia iliaca compartment block for hip fractures in the emergency department. J. Emerg. Med. 2012; 43: 692–697. DOI: 10.1016/j.jemermed.2012.01.050.
- Desmet M., Vermeylen K., Van Herreweghe I., Carlier L., Soetens F., Lambrecht S., Croes K., Pottel H., Van de Velde M. A longitudinal supra-inguinal fascia iliaca compartment block reduces morphine consumption after total hip arthroplasty. Reg Anesth. Pain Med. 2017; 42: 327–333. DOI: 10.1097/AAP.0000000000000543.
- Zhang X.Y., Ma J.B. The efficacy of fascia iliaca compartment block for pain control after total hip arthroplasty: A meta-analysis. J. Orthop. Surg. Res. 2019; 66: 89–98. DOI: 10.1186/s13018-018-1053-1.
- Bohringer C., Astorga C., Liu H. The benefits of opioid free anesthesia and the precautions necessary when employing it. Transl. Perioper. Pain Med. 2020; 7: 152–157.
- Ayoo K., Mikhaeil J., Huang A., Wąsowicz M. The opioid crisis in North America: Facts and future lessons for Europe. Anaesthesiol Intensive Ther. 2020; 52: 139–147. DOI: 10.5114/ait.2020.94756.
- Gao Y., Tan H., Sun R., Zhu J. Fascia iliaca compartment block reduces pain and opioid consumption after total hip arthroplasty: A systematic review and meta-analysis. Int. J. Surg. 2019; 65: 70–79. DOI: 10.1016/j.ijsu.2019.03.014.
- Zhang X.Y., Ma J.B. The efficacy of fascia iliaca compartment block for pain control after total hip arthroplasty: A meta-analysis. J. Orthop. Surg. Res. 2019; 66: 89–98. DOI: 10.1186/s13018-018-1053-1.
НЕТ E-MAIL И ORCID АВТОРОВ
Крылов Сергей Валерьевич, к.м.н., зав. отделением анестезиологии – реанимации № 21, доцент кафедры анестезиологии и реаниматологии2
Пасечник Игорь Николаевич, д.м.н., проф., гл. внештатный специалист по анестезиологии-реаниматологии Главного медицинского управления Управления делами Президента России, зав. кафедрой анестезиологии и реаниматологии2
Гужев Сергей Сергеевич, врач – анестезиолог-реаниматолог отделения анестезиологии – реанимации № 21, ассистент кафедры анестезиологии и реаниматологии2
Орлецкий Анатолий Корнеевич, д.м.н., проф., лауреат премии правительства России в области науки, заслуженный врач РФ, зав. отделением спортивной травмы № 41
Шумский Алексей Андреевич, к.м.н., врач – травматолог-ортопед отделения спортивной травмы № 41
Дгебуадзе Георгий, врач – травматолог-ортопед отделения спортивной травмы № 41
Герасенкова Анастасия Дмитриевна, врач – травматолог-ортопед, аспирант1
1ФГБУ «Национальный медицинский исследовательский центр травматологии и ортопедии имени Н.Н. Приорова» Минздрава России, Москва
2ФГБУ ДПО «Центральная государственная медицинская академия» Управления делами Президента Российской Федерации, Москва
Автор для переписки: Крылов Сергей Валерьевич. E-mail: doc087@inbox.ru
Krylov Sergey V., PhD Med, head of Dept of Anesthesiology and Intensive Care No. 21, associate professor at Dept of Anesthesiology and Resuscitation2
Pasechnik Igor N., DM Sci (habil.), professor, chief freelance specialist in anesthesiology and resuscitation of the Main Medical Directorate of the Presidential Administration of the Russian Federation, head of Dept of Anesthesiology and Resuscitation2
Guzhev Sergey S., anesthesiologist-resuscitator at Dept of Anesthesiology and Intensive Care No. 21, assistant at Dept of Anesthesiology and Resuscitation2
Orletsky Anatoly K., DM Sci (habil.), professor, laureate of the Prize of the Government of Russia in the field of science, honored doctor of the Russian Federation, head of Sports Injury Dept No. 41
Shumsky Aleksey A., PhD Med, traumatologist-orthopedist at Sports Injury Dept No. 41
Dgebuadze Georgy, traumatologist-orthopedist at Sports Injury Dept No. 41
Gerasenkova Anastasia D., traumatologist-orthopedist, postgraduate student1
1National Medical Research Center for Traumatology and Orthopedics n.a. N.N. Priorov, Moscow, Russia
2Central State Medical Academy, Moscow, Russia
Corresponding author: Krylov Sergey V. E-mail: doc087@inbox.ru

