Ю.А. Сергеев¹, А.А. Долгалев¹, Д.З. Чониашвили², В.М. Аванисян1
¹ ФГБОУ ВО «Ставропольский̆ государственныӗ медицинский университет» Министерства здравоохранения РФ, г. Ставрополь, Российская Федерация.
² ФГБОУ ВО «Северо-Осетинский государственный университет имени Коста Левановича Хетагурова» (СОГУ), г. Владикавказ, Российская Федерация.
Аннотация
Введение. Разработка новых дентальных имплантатов в условиях бурно развивающейся отечественной промышленности позволяет найти альтернативные возможности при лечении клинически сложных ситуаций, подобрать необходимое индивидуальное решение при проведении операции дентальной имплантации, а соответственно выполнить операцию безошибочно, и достичь желаемых результатов. Однако разработка дентального имплантата является сложным многоступенчатым процессом, в связи с чем необходимо досконально изучить как характеристики материала, из которого изготавливается имплантат, так и его биофизические особенности до момента его интеграции в костную ткань.
Цель работы: по данным литературных источников оценить возможности и особенности применения метода конечных элементов при разработке новых систем дентальных имплантатов.
Материал и методы. Был проведен поиск в отечественных электронных библиотеках e-library, «КиберЛенинка», а также PubMed, Medline, Web of Science и Google Scholar по следующим ключевым словам: дентальный имплантат, конечно-элементный анализ, математическая модель. Было отобрано и проанализировано 66 работ.
Результаты. Метод конечных элементов является точным методом анализа разрабатываемого имплантата, однако имеет определенные ограничения, так как в конечно-элементной сетке граница раздела имплантата и кости представляет собой непрерывную связь. Отсутствие микродвижения на границе имплантата и кости во время нагрузки, в действительности отличается от реальной клинической ситуации. Ожидаемая 100% остеоинтеграция на основании 3D-моделирования не может быть идеальным вариантом и никогда не соответствует реальности в клинической ситуации. Однако, использование метода конечных элементов позволяет протестировать одиночные нагрузки и углы наклона, что в клинической ситуации проявляется крайне редко.
Ключевые слова: биосовместимость, остеоинтеграция, биомеханика, дентальный имплантат, конечно-элементный анализ, математическая модель.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Контактное лицо: Сергеев Юрий Андреевич, заочный аспирант кафедры стоматологии общей практики и детской стоматологии ФГБОУ ВО «Ставропольский государственный медицинский университет», Ставрополь, ул. Мира 310, Российская Федерация. Для переписки: serg_yuriy@mail.ru, tel. +7-906-440-18-89
APPLICATION OF THE FINITE ELEMENT ANALYSIS IN THE DEVELOPMENT OF NEW DENTAL IMPLANT SYSTEMS
Yu.A. Sergeev¹, A.A. Dolgalev¹, D.Z. Choniashvili², V.M. Avanisyan1
¹ Stavropol State Medical University of the Ministry of Health of the Russian Federation, Stavropol, Russian Federation
² Federal State Budgetary Educational Institution of Higher Professional Education «Kosta Khetagurov North Ossetian State University» (NOSU), Vladikavkaz, Russian Federation
Abstract
Introduction. The development of new dental implants in the context of the booming domestic industry makes it possible to find alternative options in the treatment of clinically difficult situations, to select the necessary individual solution during dental implant surgery, and consequently, to perform the surgery in an error-free manner and achieve the desired results. The development of a dental implant is a multistep process, and the characteristics of the implant material and its biophysical characteristics must be studied in detail until the implant is integrated into the bone tissue.
The aim of the study: to estimate the opportunities and prospects of applying the finite elements method by developing the new systems of dental implants according to the literature data.
Material and methods. A search was carried out in the national digital libraries e-library, CyberLeninka, as well as PubMed, Medline, Web of Science and Google Scholar using the following keywords: dental implant, finite-element analysis, mathematical model. Sixty-nine papers were selected and analysed.
Results. The finite element method is an accurate method to analyse the implant being developed, but it has certain limits, because in the finite element mesh, the implant-bone interface is a continuous relationship. The absence of micro-movement at the implant-bone interface during loading is different from the actual clinical situation. The expected 100% osseointegration based on 3D-modelling can’t be an ideal option and never corresponds to the reality in the clinical situation. However, the use of the finite element method makes it possible to test single loads and inclination angles, which in the clinical situation is very rare.
Keywords: biocompatibility, osseointegration, biomechanics, dental implant, finite element analysis, mathematical model.
Conflict of interest. The authors declare no conflict of interest.
Contact person: Yuriy Andreevich Sergeev, Postgraduate Student, Department of General Practice and Pediatric Dentistry, Stavropol State Medical University of the Ministry of Health of the Russian Federation, 310 Mira Street, Stavropol, Russian Federation. For correspondence: serg_yuriy@mail.ru, tel. +7-906-440-18-89.
Введение
На сегодняшний день вопросам, связанным с достижением положительных результатов при операции дентальной имплантации, уделяется значительное внимание. Обусловлено это расширением ряда методик, способов проведения оперативного вмешательства, широким ассортиментом врача стоматолога-хирурга, особенно с учётом повсеместного развития и внедрения цифровой стоматологии, а также новыми видами имплантатов [1, 2].
Принято считать, что в момент разработки дентального имплантата изучение биофизических характеристик традиционно занимает первостепенное значение. Обусловлено это рядом факторов, к числу которых несомненно стоит отнести реакцию костной ткани на чужеродное тело, соотношение нагрузки дентального имплантата и кости, а также особенности распределения сил на имплантат-абатментовом соединении. При этом, применительно к дентальным имлантатам, следует фиксировать следующие особенности:
- характер разрушения: усталостное или временное (статическое);
- состояние кости, как в месте установки самого имплантата, так и окружающей костной ткани;
- состояние узлов фиксации имплантата;
- степень остеоинтеграции имплантата на разных участках
В сумме знаний, необходимых дентальному имплантологу, применяющему дентальный имплантат, особую роль приобретают основы биомеханического обоснования принимаемых решений [3].
Недостаточный биомеханический анализ при конструировании, изготовлении и применении дентальных имплантатов может привести к отсутствию образования интерфейса кость-имплантат, а также недолговечности их функционирования, что в свою очередь скажется на состоянии пациента и повлечет за собой негативные отзывы.
Целью работы явилось изучение доступных в электронных библиотеках публикаций, включавших информацию о возможностях и особенностях применения метода конечных элементов при разработке новых систем дентальных имплантатов.
Материалы и методы исследования
При изучении данного вопроса были проанализировали научные источники, индексируемые в PubMed, Medline, Web of Science и Google Scholar. В источниках, описывающих оригинальные исследования в этой области, акцент был сделан на прототипах разрабатываемых имплантатов, распределении напряжений на прилегающую кость, биомеханику зубного имплантата и кости, а также сопряжение имплантата и кости.
Результаты и выводы
Зубные имплантаты из титана (Ti) и его сплавов (роксолид, сплав титана с цирконием и т.д.) являются одной из самых надежных альтернатив для замещения отсутствующих зубов за счёт своих оптимальных биомеханических свойств [66,68]. Практически все существующие имплантаты производятся из титана, который обладает твердой структурой, и более высокой прочностью, которая в 5–10 раз превышает прочность кости [4]. Стоит отметить, что значительное несоответствие прочности имплантата и кости может способствовать возникновению перегрузки, асептическому воспалению и резорбции кости [5,6,7,8,9,10].
На данный момент разработка новых систем дентальных имплантатов основывается на принципах оптимизации физической плотности имплантата и имитации костной ткани [11,12,13,14,15,16] для преодоления вышеупомянутых осложнений и достижения полноценного ремоделирования костной ткани.
Так, на данный процесс могут влиять многие факторы, такие как материал и конструкция имплантата [17,18,19,20,21], поверхность имплантата [22,23,24,25] и качество кости [9,26,27,28,29].
Имплантаты обладают большей физической плотностью и способнывоспринимать большую нагрузку и переносить меньше напряжений и деформаций на окружающую костную ткань. Величина деформации в окружающей кости определяет процесс ремоделирования при окклюзионных нагрузках [30,31], что доказано трансформационным законом Вольфа.
Гарольд Фрост [32] описал теорию механостата как изменение уровня деформации и соответствующие изменения плотности костной ткани. Плотность костной ткани — это величина, которая часто используется для оценки клинических данных о здоровье костей. У каждого человека может быть разная плотность костной ткани. Кроме того, плотность костной ткани варьируется в разных возрастных и гендерных группах [33].
Чтобы преодолеть вышеупомянутые осложнения, многие исследователи работают над разработкой новых материалов и биоинспирированных конструкций и структур с использованием как стандартных решений, так и аддитивных технологий (3D-печати) с целью воссоздания механических свойств, хорошо совместимых с костной тканью [23,34,35,36]. Для моделирования различных плотностей костной ткани, конструкций имплантатов и различных механических нагрузок, активно применяются компьютерные методы в оценке биомеханики имплантатов [37,38]. Наиболее актуальным методом моделирования и расчёта прочности и надежности разрабатываемых изделий является использование современных пакетов автоматизированного инженерного анализа, при этом наиболее эффективной CAE-системой, используемой для моделирования процессов функционирования подобных изделий, является программа ANSYS [39].
Основным методом компьютерного моделирования является метод конечно-элементного анализа (МКЭ), который позволяет рассчитывать напряженно-деформированное состояние (НДС), возникающее внутри механической системы под воздействием внешних сил, а также отображает участки конструкции, где происходит деформация материала и последующее разрушение [40]. НДС, рассчитанное методом конечно-элементного анализа, может не превышать предельных значений напряжений.
Важно учитывать, что передача напряжения между имплантатом и костью зависит от ряда факторов и описание этого процесса довольно объемное. Для реализации биомеханического воздействия используется математическая 3D-модель, в которой определены геометрические данные имплантата, механические свойства кости и параметры интерфейса кости-имплантат, иначе называемая сетью конечных элементов [41-44]. Путем изменения отдельных элементов данной системы возможно получить данные о клинической эффективности дентального имплантата.
Так при изучении биомеханических особенностей дентальных имплантатов возможно полноценно определить биомеханические изменения и НДС, что в свою очередь будет способствовать дальнейшему совершенствованию методов имплантации и повышать эффективность проводимого лечения [45].
В момент создания дентального имплантата активно используют методы биомеханической оценки его влияния на интерфейс кость-имплантат, дабы предсказать поведение имплантата непосредственно в костной ткани и оценить его преимущества и недостатки [46]. Для изучения биомеханического воздействия используется компьютерная модель (Рисунок 1) с заранее определенными техническими характеристиками дентального имплантата для последующего построения в цифровом виде конечно-элементной модели участка челюсти с дентальным имплантатом (параметры костной ткани определяются заранее исходя из уже имеющихся данных).

Рис. 1. Зубные имплантаты (а) и 3D-модель нижней челюсти с зубными имплантатами с абатментами (б)
Одна из первых работ по применению метода конечных элементов для проведения биомеханического анализа в стоматологии была отражена Korioth, T.W.and Hannam, A.G. [44]. Позже Van Staden, R.C. et al. [47] в работе обозначили, что МКЭ следует считать численным методом анализа деформаций и напряжений в любой заданной структуре. На сегодняшний день МКЭ является широко используемым методом в области стоматологической биомеханики [48].
Исследование на базе метода конечных элементов (МКЭ) с использованием упрощенных моделей, позволяет обеспечить «чистоту эксперимента», т.е. исключить все несущественные факторы, присущие реальному объекту, при этом свойства моделей с МКЭ максимально приближенны к реальному объекту [49].
На этапе разработки дентального имплантата конечно-элементная модель используется для оценки технических характеристик и в подавляющем случае будет состоять из нескольких частей (Риунок 2), а именно челюстной кортикальной кости, челюстной трабекулярной кости, дентального имплантата, абатмента и абатментного винта, а также коронки и её способа фиксации [9, 46,50].
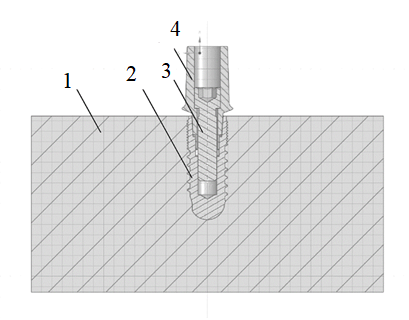
Рис. 2. Конечно-элементная модель при разработке дентального имплантата: 1 — блок костной ткани, 2 — тело имплантата, 3 – винт, 4 – абатмент
При этом заранее необходимо обозначить свойства материалов дентальных имплантатов, которые будут использованы при моделировании биомеханики. Необходимо чтобы материалы были однородными, изотропными и линейно-упругими. В связи с чем для обозначения свойств материалов зачастую используются 2 независимых параметра (модуль Юнга (E) и коэффициент Пуассона (ν)).
Элемент сетки, используемый в конечно-элементной компьютерной модели, представляет собой тетраэдрическую сетку [51,52] (Рисунок 3).
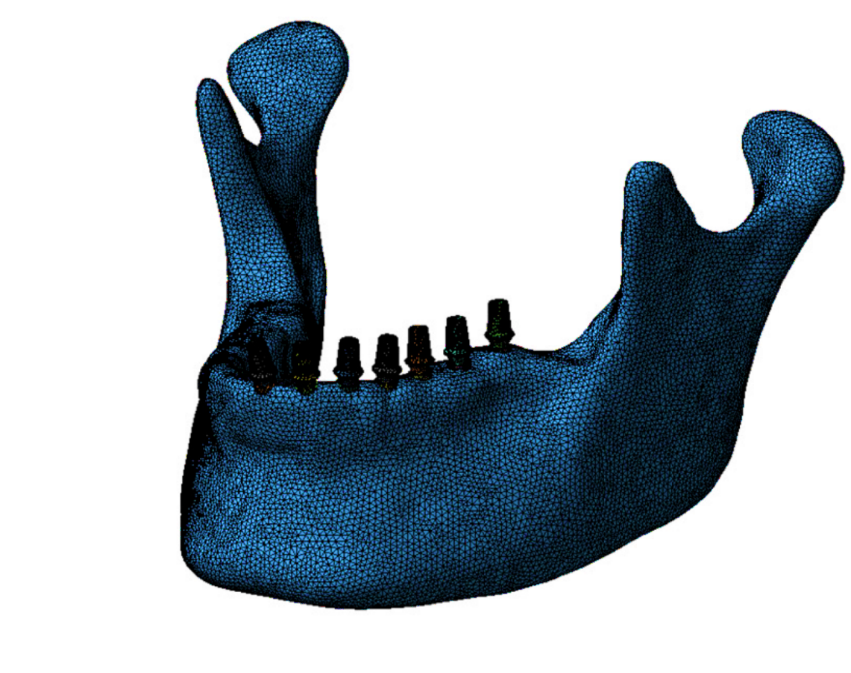
Рис. 3. Элемент сетки в компьютерной модели
В большинстве случаев при определении влияния тех или иных сил необходимо использовать модель конечно-элементной сетки для определения различных условий окклюзии на систему разрабатываемых дентальных имплантатов.
МКЭ позволяет оценить распределение сил реакции и структурного напряжения на фиксированном верхнем конце абатмента в системе зубных имплантатов [20,53].
Используя математическую модель, можно оценить распределение напряжения фон Мизеса в смоделированном участке кости (Рисунок 4). Более того, при изучении нагрузки на альвеолярную кость в областях одного зуба можно увидеть, что участки в связи с кортикальной костью имеют более высокую нагрузку. Возникновение этого высокого напряжения можно объяснить законом Гука (напряжение = модуль Юнга × деформации). Когда система зубных имплантатов получает внешнюю силу, она будет иметь небольшое смещение вниз, сжимая альвеолярную кость и создавая такое же смещение на стыке кортикальной кости и трабекулярной кости (создавая здесь ту же деформацию) [12]. При этом напряжение пропорционально модулю Юнга. Таким образом, кортикальная кость над альвеолярной костью имеет более высокую нагрузку [54]. Поэтому при конструкции некоторых имплантатов увеличивается количество витков микрорезьбы на шейке имплантата, увеличивая площадь его контакта с поверхностью альвеолярной кости, предотвращая ослабление системы зубных имплантатов при воздействии внешних сил, тем самым повышая успешность имплантации.
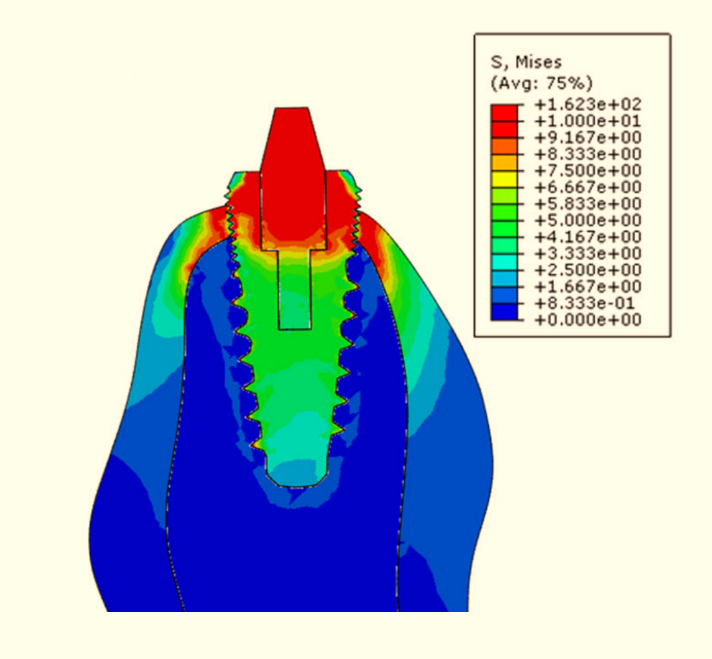
Рис. 4. Распределение нагрузки фон Мизеса
Распределение нагрузки фон Мизеса на систему кость-имплантат показывает, что высокие нагрузки на зубные имплантаты под воздействием внешних сил в основном возникают вблизи шейки зубного имплантата, где зубной имплантат контактирует с абатментом. Поэтому, когда зуб получает внешнюю силу, он непосредственно деформирует шейку зубного имплантата. Согласно закону Гука, в этой области будет генерироваться высокий стресс. [10].
Стоит отметить, что альвеолярная кость, прилегающая к имплантатам, на которые воздействовали внешние силы, также будет испытывать высокие нагрузки из-за деформации [44].
При оценке напряжения на абатменте и абатментном винте можно увидеть, что высокая нагрузка на абатмент возникает при его стыке с зубным имплантатом [55,56]. Высокая нагрузка на абатментный винт возникает в области, где головка винта соединена с абатментом, также соответствующая области, где геометрическая форма головки винта и винта изгибается. Поэтому конструкция абатментов и абатментных винтов должна избегать генерации высоких напряжений геометрической формой. В противном случае, поскольку пациент будет продолжительное время пользоваться конструкцией, система зубных имплантатов может быть повреждена из-за усталости материалов [57,58].
При получении уникальных моделей стоматологических имплантатов, а именно на этапе их разработки на сегодняшний день используют самоадаптивную 3D-модель, которая в отличии от традиционных подходов в параметризованном самоизменяющейся модели имплантата, сборке самоадаптивных 3D-моделей, передаче двунаправленных параметров и настройках переменных [59].
Построение параметризованной самоизменяющейся модели имплантата означает, что модель имплантата строится на основе диаметра и длины имплантата. Другими словами, количество резьбы имплантата может изменяться с автоматическим изменением диаметра и длины имплантата. Сборка самоадаптивных 3D-моделей означает, что все модели перестраиваются на основе параметров имплантата. То есть параметры других частей (типы костей) изменялись при автоматических изменениях параметров имплантата [4,58].
Средства передачи двунаправленных параметров CAD (Pro/E) и CAE (Ansys Workbench) могут передавать параметры модели взаимно и бесшовно. Настройки переменных включают входные переменные (D и L) и выходные переменные (max EQV напряжение в нижней челюсти и максимальное смещение в импланто-абатментном комплексе) [38,39].
Результаты
МКЭ является точным методом анализа разрабатываемого имплантата, однако имеет определенные ограничения, так как в конечно-элементной сетке граница раздела имплантата и кости представляет собой непрерывную связь. Отсутствие микродвижения на границе имплантата и кости во время нагрузки, в действительности отличается от реальной клинической ситуации [28,60].
Ожидаемая 100% остеоинтеграция на основании 3D-моделирования не может быть идеальным вариантом и никогда не соответствует реальности в клинической ситуации. Кость (кортикальная, губчатая) и имплантат считаются изотропными и однородными, но в действительности кость анизотропна и неоднородна. Имплантат жестко закреплен в кости. Нагрузки были приложены только в точечных местах. Продолжительность приложения силы в имплантатах и полости рта различна [8,61, 62].
Кроме того, использование МКЭ, позволяет протестировать одиночные нагрузки и углы наклона, что в клинической ситуации проявляется крайне редко [25,45, 57,63, 64, 65].
Во многих научных изысканиях с использованием метода конечных элементов большинство авторов используют оптимальные значения и нагрузки [66], однако для полноценного восприятия биомеханического поведения дентальных имплантатов необходимо акцентировать внимание на все существующие особенности моделирования биомеханики.
Выводы
Метод конечных элементов представляет из себя важный инструмент в дентальной имплантологии, так как благодаря ему возможно тестировать прототипы разрабатываемых имплантатов и исследовать особенности поведения существующих модифицированных имплантатов с целью изучения распределения напряжений на прилегающей кости, биомеханики зубного имплантата и кости, а также сопряжения имплантата и кости.
Математическая модель с учётом конечно-элементного анализа позволяет предопределить возможные риски, связанные с перегрузкой имплантата или возможными осложнениями в момент его нагружения.
Говоря об особенностях применения данного метода стоит сказать, что сочетанное использование усталостных, старческих, термических и непрерывных механических циклических нагрузок при анализе прототипов дентальных имплантатов позволяет генерировать максимально эффективные медицинские изделия с клинической точки зрения.
СПИСОК ЛИТЕРАТУРЫ
- Ananth, H.; Kundapur, V.; Mohammed, H.; Anand, M.; Amarnath, G.; Mankar, S. A review on biomaterials in dental implantology. Int. J. Biomed. Sci. 2015, 11, 113.
- Kawahara et al.//Image synthesis with deep convolutional generative adversarial networks for material decomposition in dual-energy CT from a kilovoltage CT/Comput. Biol. Med.(2021)
- Marcián P. et al.//Micro finite element analysis of dental implants under different loading conditions/Comput. Biol. Med.(2018)
- Chang, P.-K.; Chen, Y.-C.; Huang, C.-C.; Lu, W.-H.; Chen, Y.-C.; Tsai, H.-H. Distribution of micromotion in implants and alveolar bone with different thread profiles in immediate loading: A finite element study. Int. J. Oral Maxillofac. Implant. 2012, 27, e96–e101.
- Dos Santos, M.C.L.G.; Campos, M.I.G.; Line, S.R.P. Early dental implant failure: A review of the literature. Braz. J. Oral Sci. 2002, 1, 103–111.
- Han et al.//Continuous functionally graded porous titanium scaffolds manufactured by selective laser melting for bone implants/J. Mech. Behav. Biomed. Mater.(2018)
- Himmlova, L.; Dostalova, T.; Kacovsky, A.; Konvickova, S. Influence of implant length and diameter on stress distribution: A finite element analysis. J. Prosthet. Dent. 2004, 91, 20–25
- Jafari et al.//A comparative study of bone remodeling around hydroxyapatite-coated and novel radial functionally graded dental implants using finite element simulation/Med. Eng. Phys.(2022)
- Kang, X.; Li, Y.; Wang, Y.; Zhang, Y.; Yu, D.; Peng, Y. Relationships of Stresses on Alveolar Bone and Abutment of Dental Implant from Various Bite Forces by Three-Dimensional Finite Element Analysis. Biomed Res. Int. 2020, 2020, 7539628.
- Schwitalla, A.; Abou-Emara, M.; Spintig, T.; Lackmann, J.; Müller, W. Finite element analysis of the biomechanical effects of PEEK dental implants on the peri-implant bone. J. Biomech. 2015, 48, 1–7.
- Bozkaya, D.; Muftu, S.; Muftu, A. Evaluation of load transfer characteristics of five different implants in compact bone at different load levels by finite elements analysis. J. Prosthet. Dent. 2004, 92, 523–530.
- Cozzolino et al.//Implant-to-bone force transmission: a pilot study for in vivo strain gauge measurement technique/J. Mech. Behav. Biomed. Mater.(2019)
- Dutta et al.//Design of porous titanium scaffold for complete mandibular reconstruction: the influence of pore architecture parameters/Comput. Biol. Med.(2019)
- Li et al.//3D porous Ti6Al4V-beta-tricalcium phosphate scaffolds directly fabricated by additive manufacturing/Acta Biomater.(2021)
- Sato et al.//The effects of bone remodeling on biomechanical behavior in a patient with an implant-supported overdenture/Comput. Biol. Med.(2021)
- Wang Juncheng & Yang Sefei. (2017). Risk factors affecting osseointegration of implants: (eds.) Proceedings of the 8th Academic Conference of the General Stomatology Committee of the Chinese Stomatological Association (pp.338)
- Cynthia S. Petrie DDS, MS and John L. Williams PhD. Shape optimization of dental implant designs under oblique loading using the p‐version finite element method[J]. Journal of Prosthodontics, 2002, 11(4) : 333-334.
- Ghaziani A.O. et al.//The effect of functionally graded materials on bone remodeling around osseointegrated trans-femoral prostheses/J. Mech. Behav. Biomed. Mater.(2021)
- Günther F. et al.//Design procedure for triply periodic minimal surface based biomimetic scaffolds/J. Mech. Behav. Biomed. Mater.(2022)
- Verri, F.R.; de Souza Batista, V.E.; Santiago, J.F., Jr.; de Faria Almeida, D.A.; Pellizzer, E.P. Effect of crown-to-implant ratio on peri-implant stress: A finite element analysis. Mater. Sci. Eng. C 2014, 45, 234–240.
- Wu, S.-W.; Lee, C.-C.; Fu, P.-Y.; Lin, S.-C. The effects of flute shape and thread profile on the insertion torque and primary stability of dental implants. Med. Eng. Phys. 2012, 34, 797–805.
- Li et al.//Early osteointegration evaluation of porous Ti6Al4V scaffolds designed based on triply periodic minimal surface models/J. Orthop. Transl.(2019)
- Mehboob et al.//Finite element modelling and characterization of 3D cellular microstructures for the design of a cementless biomimetic porous hip stem/Mater. Des.(2018)
- Salou et al.//Enhanced osseointegration of titanium implants with nanostructured surfaces: an experimental study in rabbits/Acta Biomater.(2015)
- Shim, H.W.; Yang, B.-E. Long-term cumulative survival and mechanical complications of single-tooth Ankylos Implants: Focus on the abutment neck fractures. J. Adv. Prosthodont. 2015, 7, 423–430.
- Azcarate-Velázquez et al.//Influence of bone quality on the mechanical interaction between implant and bone: a finite element analysis/J. Dent.(2019)
- Kasani R. et al.//Stress distribution of overdenture using odd number implants – a Finite Element Study/J. Mech. Behav. Biomed. Mater.(2019)
- Peyroteo M.M.A. et al.//A mathematical biomechanical model for bone remodeling integrated with a radial point interpolating meshless method/Comput. Biol. Med.(2021)
- Piccinini et al.//Numerical prediction of peri-implant bone adaptation: comparison of mechanical stimuli and sensitivity to modeling parameters/Med. Eng. Phys.(2016)
- Негматова Д. У., Камариддинзода М. К. «Современные подходы к решению биомеханических проблем дентальной имплантологии» Вопросы науки и образования, no. 7 (53), 2019, pp. 227-234.
- Cheong V.S. et al.//Bone remodelling in the mouse tibia is spatio-temporally modulated by oestrogen deficiency and external mechanical loading: a combined in vivo/in silico study/Acta Biomater.(2020)
- Tyrovola J. B. (2015). The «Mechanostat Theory» of Frost and the OPG/RANKL/RANK System. Journal of cellular biochemistry, 116(12), 2724–2729. https://doi.org/10.1002/jcb.25265
- Gubaua J.E. et al.//Techniques for mitigating the checkerboard formation: application in bone remodeling simulations/Med. Eng. Phys.(2022)
- Santiago Junior, J.F.; Pellizzer, E.P.; Verri, F.R.; de Carvalho, P.S. Stress analysis in bone tissue around single implants with different diameters and veneering materials: A 3-D finite element study. Mater. Sci. Eng. C Mater. Biol. Appl. 2013, 33, 4700–4714.
- Yao Y. et al.//A personalized 3D-printed plate for tibiotalocalcaneal arthrodesis: design, fabrication, biomechanical evaluation and postoperative assessment/Comput. Biol. Med.(2021)
- Zheng et al.//Bone remodeling following mandibular reconstruction using fibula free flap/J. Biomech.(2022)
- Alzahrani F.S. et al.//Analytical estimations of temperature in a living tissue generated by laser irradiation using experimental data/J. Therm. Biol.(2019)
- Chakraborty et al.//Finite element and experimental analysis to select patient’s bone condition specific porous dental implant, fabricated using additive manufacturing/Comput. Biol. Med.(2020)
- Zanichelli, A., Colpo, A., Friedrich, L., Iturrioz, I., Carpinteri, A., & Vantadori, S. (2021). A Novel Implementation of the LDEM in the Ansys LS-DYNA Finite Element Code. Materials (Basel, Switzerland), 14(24), 7792. https://doi.org/10.3390/ma14247792
- Bulaqi, H.A.; Mashhadi, M.M.; Safari, H.; Samandari, M.M.; Geramipanah, F. Effect of increased crown height on stress distribution in short dental implant components and their surrounding bone: A finite element analysis. J. Prosthet. Dent. 2015, 113, 548–557.
- Kong, L.; Liu, B.; Li, D.; Song, Y.; Zhang, A.; Dang, F.; Qin, X.; Yang, J. Comparative study of 12 thread shapes of dental implant designs: A three-dimensional finite element analysis. World J. Model. Simul. 2006, 2, 134–140.
- Kong, L.; Zhao, Y.; Hu, K.; Li, D.; Zhou, H.; Wu, Z.; Liu, B. Selection of the implant thread pitch for optimal biomechanical properties: A three-dimensional finite element analysis. Adv. Eng. Softw. 2009, 40, 474–478.
- Koolstra, J.H.; van Eijden, T.M. Combined finite-element and rigid-body analysis of human jaw joint dynamics. J. Biomech. 2005, 38, 2431–2439.
- Korioth, T.W.; Hannam, A.G. Mandibular forces during simulated tooth clenching. J. Orofac. Pain 1994, 8, 179–189.
- Su, K.-C.; Chang, C.-H.; Chuang, S.-F.; Ng, E.Y.-K. Biomechanical evaluation of endodontic post-restored teeth—finite element analysis. J. Mech. Med. Biol. 2013, 13, 1350012.
- El-Anwar, M.I.; El-Zawahry, M.M. A three dimensional finite element study on dental implant design. J. Genet. Eng. Biotechnol. 2011, 9, 77–82.
- Van Staden, R.C.; Guan, H.; Loo, Y.C. Application of the finite element method in dental implant research. Comput. Methods Biomech. Biomed. Eng. 2006, 9, 257–270.
- Chieruzzi, M.; Pagano, S.; Cianetti, S.; Lombardo, G.; Kenny, J.M.; Torre, L. Effect of fibre posts, bone losses and fibre content on the biomechanical behaviour of endodontically treated teeth: 3D-finite element analysis. Mater. Sci. Eng. C Mater. Biol. Appl. 2017, 74, 334–346.
- Hijazi, L.; Hejazi, W.; Darwich, M.A.; Darwich, K. Finite element analysis of stress distribution on the mandible and condylar fracture osteosynthesis during various clenching tasks. J. Oral. Maxillofac. Surg. 2016, 20, 359–367.
- Baggi, L.; Cappelloni, I.; Di Girolamo, M.; Maceri, F.; Vairo, G. The influence of implant diameter and length on stress distribution of osseointegrated implants related to crestal bone geometry: A three-dimensional finite element analysis. J. Prosthet. Dent. 2008, 100, 422–431.
- Luo, D.; Rong, Q.; Chen, Q. Finite-element design and optimization of a three-dimensional tetrahedral porous titanium scaffold for the reconstruction of mandibular defects. Med. Eng. Phys. 2017, 47, 176–183.
- Su, K.-C.; Chang, C.-H.; Chuang, S.-F.; Ng, E.Y.-K. Biomechanical evaluation of endodontic post-restored teeth—finite element analysis. J. Mech. Med. Biol. 2013, 13, 1350012.
- Jo, J.-Y.; Yang, D.-S.; Huh, J.-B.; Heo, J.-C.; Yun, M.-J.; Jeong, C.-M. Influence of abutment materials on the implant-abutment joint stability in internal conical connection type implant systems. J. Adv. Prosthodont. 2014, 6, 491–497.
- Amid, R.; Ebrahimi, N.; Kadkhodazadeh, M.; Mirakhori, M.; Mehrinejad, P.; Nematzadeh, F.; Dehnavi, F. Clinical evaluation of a new device to measure maximum bite force. Dentist. Case. Rep. 2018, 2, 26–29.
- Ashley, E.T.; Covington, L.L.; Bishop, B.G.; Breault, L.G. Ailing and failing endosseous dental implants: A literature review. J. Contemp. Dent. Pract. 2003, 4, 35–50.
- Li, T.; Hu, K.; Cheng, L.; Ding, Y.; Ding, Y.; Shao, J.; Kong, L. Optimum selection of the dental implant diameter and length in the posterior mandible with poor bone quality–A 3D finite element analysis. Appl. Math. Model. 2011, 35, 446–456.
- Мураев А. А., Иванов С. Ю., Леонов С. В. [и др.] // Сравнительный анализ биомеханики при различных узлах сопряжения имплантата и абатмента на основании данных трехмерного конечно-элементного моделирования / Стоматология. – 2019. – Т. 98. – № 1. – С. 11-16. – DOI 10.17116/stomat20199801111.
- Chang, Y.-H.; Chan, M.-Y.; Hsu, J.-T.; Hsiao, H.-Y.; Su, K.-C. Biomechanical Analysis of the Forces Exerted during Different Occlusion Conditions following Bilateral Sagittal Split Osteotomy Treatment for Mandibular Deficiency. Appl. Bionics Biomech. 2019, 2019, 4989013.
- Ryu, H.-S.; Namgung, C.; Lee, J.-H.; Lim, Y.-J. The influence of thread geometry on implant osseointegration under immediate loading: A literature review. J. Adv. Prosthodont. 2014, 6, 547–554.
- Hansson, S. A conical implant–abutment interface at the level of the marginal bone improves the distribution of stresses in the supporting bone: An axisymmetric finite element analysis. Clin. Oral Implant. Res. 2003, 14, 286–293.
- Huang, H.-L.; Hsu, J.-T.; Fuh, L.-J.; Tu, M.-G.; Ko, C.-C.; Shen, Y.-W. Bone stress and interfacial sliding analysis of implant designs on an immediately loaded maxillary implant: A non-linear finite element study. J. Dent. 2008, 36, 409–417.
- Marcián, P.; Borák, L.; Valášek, J.; Kaiser, J.; Florian, Z.; Wolff, J. Finite element analysis of dental implant loading on atrophic and non-atrophic cancellous and cortical mandibular bone–a feasibility study. J. Biomech. 2014, 47, 3830–3836.
- Савранский Ф. З., Гришин П. О., Кушнир Е. Н. [и др.] // Использование метода математического моделирования напряженно- деформированного состояния костной ткани при дентальной имплантации (литературный обзор) / Современная ортопедическая стоматология. – 2018. – № 30. – С. 30-33.
- Huang, H.-L.; Su, K.-C.; Fuh, L.-J.; Chen, M.Y.; Wu, J.; Tsai, M.-T.; Hsu, J.-T. Biomechanical analysis of a temporomandibular joint condylar prosthesis during various clenching tasks. J. Cranio-MaxilloFac. Surg. 2015, 43, 1194–1201.
- Van Eijden, T. Three-dimensional analyses of human bite-force magnitude and moment. Arch. Oral Biol. 1991, 36, 535–539.
- Merdji et al.//Stress distribution in dental prosthesis under an occlusal combined dynamic loading/Mater. Des.(2012)
ИНФОРМАЦИЯ ОБ АВТОРАХ
- Сергеев Юрий Андреевич, заочный аспирант кафедры стоматологии общей практики и детской стоматологии ФГБОУ ВО «Ставропольский государственный медицинский университет», Ставрополь, ул. Мира 310, Российская Федерация. ORCID: https://orcid.org/0000-0002-6183-2586. Тел. +7-906-440-18-89, e-mail: serg_yuriy@mail.ru.
- Долгалев Александр Александрович, доктор медицинских наук, профессор кафедры стоматологии общей практики и детской стоматологии, начальник центра инноваций и трансфера технологий научно-инновационного объединения, ФГБОУ ВПО «Ставропольский государственный медицинский университет» Министерства здравоохранения РФ. Профессор кафедры клинической стоматологии с курсом ХС и ЧЛХ Пятигорского медико-фармацевтического института – филиал Волгоградского государственного медицинского университета, Ставрополь, Российская Федерация. ORCID: https://orcid.org/0000-0002-6352-6750. Тел. +7-962-440-48-61, e-mail: dolgalev@dolgalev.pro
- Чониашвили Давид Зурабович, кандидат медицинских наук, доцент кафедры терапевтической, хирургической и детской стоматологии с курсом имплантология, реконструктивная хирургия полости рта, детская ЧЛХ, декан медицинского факультета ФГБОУ ВО «Северо-Осетинский государственный университет имени Коста Левановича Хетагурова» (СОГУ), главный врач Клинико-диагностического центра стоматологии СОГУ, Владикавказ, Российская Федерация. Тел.+7-918-828-11-72, e-mail: davidchoniashvili@mail.ru
- Аванисян Вазген Михайлович, ординатор 1 года обучения кафедры терапевтической стоматологии ФГБОУ ВПО «Ставропольский государственный медицинский университет» Министерства Здравоохранения Российской Федерации, 355000, г. Ставрополь, Российская Федерация. ORCID: https://orcid.org/0000-0002-0316-5957, SPIN-код: 1207-9234. Teл. +7-928-633-89-95, e-mail: avanvaz@yandex.ru
INFORMATION ABOUT AUTHORS
- Sergeev Yuriy Andreevich, Postgraduate Student, Department of General Practice and Pediatric Dentistry, Stavropol State Medical University of the Ministry of Health of the Russian Federation, 355000, Stavropol, Russian Federation. ORCID: https://orcid.org/0000-0002-6183-2586. Tel. +7-906-440-18-89, e-mail: serg_yuriy@mail.ru.
- Dolgalev Alexander Alexandrovich, MD, Head of the Center for Innovation and Technology Transfer, Professor of the Department of General Practice Dentistry and Pediatric Dentistry of the Stavropol State Medical University of the Ministry of Health of the Russian Federation, Professor of the Department of Clinical Dentistry with a course of OS and MFS of the Pyatigorsk Medical and Pharmaceutical as Institute-branch of the Volgograd State Medical University Stavropol, Russian Federation. ORCID: https://orcid.org/0000-0002-6352-6750. Tel. +7-962-440-48-61, e-mail: dolgalev@dolgalev.pro
- Choniashvili David Zurabovich, Candidate of Medical Sciences, Associate Professor of the Department of Therapeutic, Surgical and Pediatric Dentistry with courses in Implantology, Reconstructive Oral Surgery, Pediatric maxillofacial surgery, Dean of the Medical Faculty of the Federal State Educational Institution of Higher Professional Education «North Ossetian State University named after Kosta Levanovich Khetagurov (NOSU), Head Doctor of the Clinical and Diagnostic Center of Dentistry of NOSU, Vladikavkaz, Russian Federation. Tel. +7-918-828-11-72, e-mail: davidchoniashvili@mail.ru
- Avanisyan Vazgen Mikhailovich, 1-st year resident at the Department of Therapeutic Dentistry, Stavropol State Medical University of the Ministry of Health of the Russian Federation, 355000, Stavropol, Russian Federation. ORCID: https://orcid.org/0000-0002-0316-5957, SPIN code: 1207-9234. Tel. +7-928-633-89-95, e-mail: avanvaz@yandex.ru
Статья опубликована в Научном журнале «Медицинский алфавит» в перечне ВАК (II Квартиль), серия Стоматология (1)2023

