Н. В. Теплова1, М. В. Путилина1, Г. А. Червякова1, В. В. Апокина1, А. В. Никифорова2
1ФГАОУ ВО «Российский национальный исследовательский медицинский университет имени Н. И. Пирогова» Минздрава России, Москва
2ФГБНУ «Научно-исследовательский институт ревматологии имени В. А. Насоновой», Москва
РЕЗЮМЕ
Ревматическая полимиалгия (РПМА) – это воспалительное заболевание костно-мышечной системы, которое редко диагностируется у пациентов старше 50 лет. РПМА характеризуется болью и продолжительной утренней скованностью в плечевом, тазовом поясе и шее. На сегодняшний день не существует единого клинического, лабораторного или инструментального признака, наличие которого позволило бы подтвердить диагноз. Основой метод лечения – пероральная терапия глюкокортикостероидами. К альтернативным вариантам лечения относится стероидосберегающая терапия (метотрексат, тоцилизумаб). Для уменьшения болей возможно применение НПВП.
КЛЮЧЕВЫЕ СЛОВА: ревматическая полимиалгия, глюкокортикостероиды, метотрексат, тоцилизумаб, НПВП.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы заявляют об отсутствии конфликта интересов.
Difficulties in differential diagnosis and modern approaches to treatment of polymyalgia rheumatica
N. V. Teplova1, M. V. Putilina1, G. A. Chervyakova1, V. V. Apokina1, A. V. Nikiforova2
1Pirogov Russian National Research Medical University, Moscow, Russia
2V. A. Nasonova Research Institute of Rheumatology, Moscow, Russia
SUMMARY
Polymyalgia rheumatica (RPMA) is an inflammatory disease of the musculoskeletal system that is rarely diagnosed in patients over 50 years of age. RPMA is characterized by pain and prolonged morning stiffness in the shoulder, pelvic girdle, and neck. To date, there is no single clinical, laboratory or instrumental sign, the presence of which would confirm the diagnosis. The main method of treatment is oral therapy with glucocorticosteroids. Alternative treatment options include steroid-sparing therapy (methotrexate, tocilizumab). NSAIDs may be used to reduce pain.
KEY WORDS: polymyalgia rheumatica, glucocorticosteroids, methotrexate, tocilizumab, NSAIDs. CONFLICT OF INTEREST. The authors declare no conflict of interest.
Введение
Ревматическая полимиалгия (РПМА) – системное воспалительное заболевание неясной этиологии, встречающееся у людей пожилого возраста (чаще женщин) с сопутствующей патологией (АГ, ЦВЗ) и характеризующееся болями и скованностью мышц плечевого и (или) тазового пояса,
часто сочетающееся с височным артериитом [1–4]. Пик заболеваемости приходится на возраст от 65 до 70–80 лет [3, 4]. Несмотря на то что РП встречается по всему миру, распространенность заболевания отличается в разных регионах. Наиболее высокая заболеваемость на 100 тысяч человек в возрасте 50 лет и старше наблюдается в скандинавских и северных европейских странах: в Дании – 68,00, в других Скандинавских странах – 58,70, в Италии – 12,70, в Японии – 1,47 [5, 6].
Этиология и патогенез
Этиологические факторы РПМА остаются неизвестными. Вероятно, главную роль в развитии заболевания играют изменения иммунной системы при воздействии ряда факторов (инфекции, генетическая предрасположенность и т. д.) [6].
Инфекционные факторы (вирус или бактерии) могут вызывать активацию воспалительных процессов,
чаще аутоиммунных, которые индуцируют проявления РПМА [7, 8]. Хотя рядом авторов была описана связь заболевания с эпидемиями, вызванными микоплазмами, парвовирусом B19, хламидиями, в более крупных исследованиях такая связь не была подтверждена [8, 9]. Аденовирус и респираторно-синцитиальный вирус могут быть пусковыми механизмами развития РПМА, особенно у пожилых людей [10]. Cimmino и соавт. обнаружили антитела к аденовирусу (ADV) и респираторно-синцитиальному вирусу (RSV) у пациентов с РПМА [11].
Генетические факторы. Доказана связь между заболеванием и специфическими полиморфизмами генов, связанных с иммунной регуляцией. Несколько аллелей HLA-DRB 1 связаны с повышенной частотой воспаления в суставах, как это наблюдается при ревматоидном артрите [12]. Salvarani и соавт. сообщили о ассоциации между аллелями HLA-DRB 1*04 и изолированной РПМА среди своих итальянских пациентов [13]. Gonzalez Gay и соавт. также предположили возможное влияние аллелей HLADRB 1*04 на развитие более тяжелого течения РПМА за счет выраженного синовиального воспаления [14].
Патогенез РПМА. Активация врожденной и адаптивной иммунных систем в ответ на неизвестные триггеры окружающей среды является ключевым патогенетическим механизмом РПМА [15]. РПМА представляет собой антиген-опосредованную болезнь с локальной Т-клеточной и макрофагальной активацией с избыточной продукцией цитокинов, а именно ИЛ-1 и ИЛ-6, вызывающих системное воспаление с высоким острофазовым ответом [16–18]. ИЛ-6 активируют T-хелперы (Th17). Th17 ассоциированы с аутоиммунными процессами [16]. Активированные Т-хелперы, такие как Th1, Th2 и Th17, обнаруживаются в синовиальной полости суставов при ревматоидном артрите [15]. Т-клетки проникают в артерии через vasa vasorum и взаимодействуют с дендритными клетками, которые, в свою очередь, регулируют активацию Т-клеток и макрофагов. Цитокины, продуцируемые T-клетками, контролируют дифференциацию инфильтрирующих макрофагов [19]. У пациентов с различными хроническими воспалительными заболеваниями наблюдается значительная несоответствующая возрасту экспансия CD4+ CD28 – Т-клеток, что позволяет предположить, что эти клетки играют роль в их патогенезе. CD4+CD28 – T-клетки могут продуцировать большое количество провоспалительных цитокинов, таких как IFN-γ и TNF-α, а также обладают цитотоксическим потенциалом, который может вызывать повреждение тканей и развитие патогенеза при многих воспалительных заболеваниях [15]. Воспаление возникает на уровне синовиальной оболочки и сумок, связанных с плечевым и тазобедренным поясами, где происходит распознавание неизвестного антигена дендритными клетками или макрофагами (рис. 1) [15]. В здоровой иммунной системе чрезмерная стимуляции регулируется с помощью отрицательных костимулирующих сигналов, которые снижают реактивность тканей. Белок запрограммированной гибели клеток – 1, также известный как PD-1 и CD279 (кластер дифференцировки 279), представляет собой рецептор клеточной поверхности, который играет важную роль в регуляции гомеостаза иммунной системы, подавляя воспалительную активность Т-клеток. PD-1 способствует апоптозу антигенспецифических Т-клеток в лимфатических узлах, одновременно уменьшая апоптоз регуляторных Т-клеток [19].
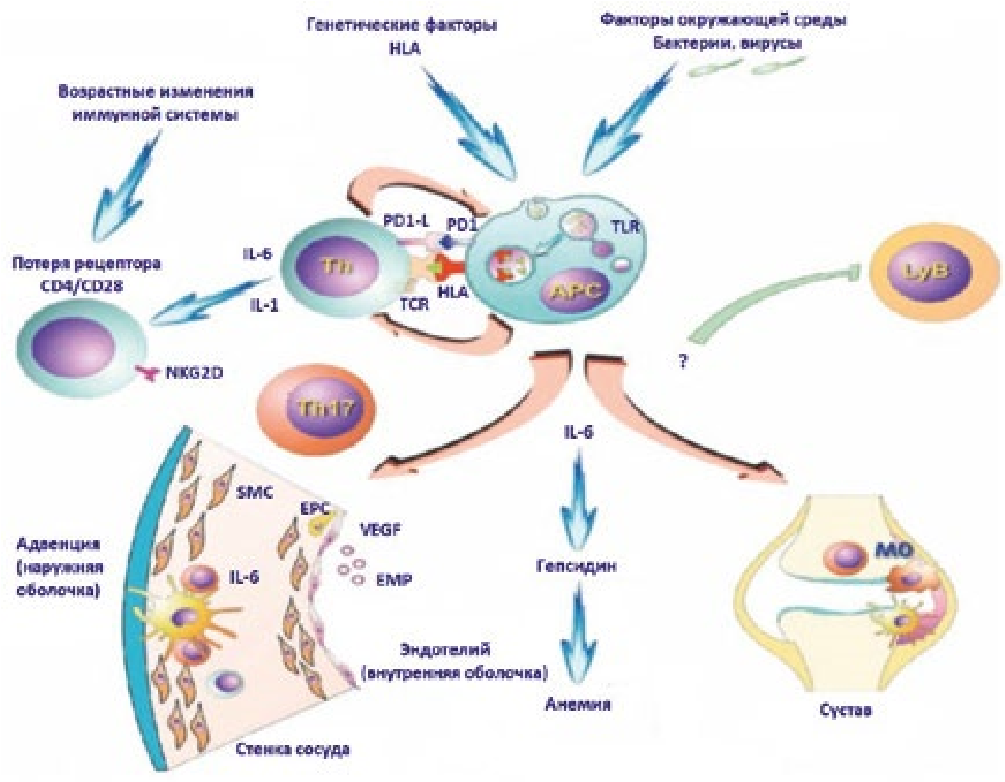
Рисунок 1. Патогенетические механизмы развития ревматической полимиалгии (перевод с англ.) [7]
Примечания: LyB – В-лимфоцит; TLR (toll-like receptor) – толл-подобный рецептор; APC (antigen-presenting cell) – антиген-презентирующая клетка; PD1 (programmed cell death protein-1) – белок запрограммированной гибели клеток – 1; PD1-L – лиганд белка запрограммированной гибели клеток; TCR (T-cell receptor) – Т-клеточный рецептор; Th17 – Т-хелпер 17; CD4/CD28 – кластер дифференцировки 4/28;
NKG2D – рецептор естественных киллеров; IL-1, IL-6 – интерлейкины -1,-6;
SMC (structural maintenance of chromosomes) – белок структурной поддержки хромосом; EPC (endothelial progenitor cell) – эндотелиальная клетка-предшественница; VEGF (vascular endothelial growth factor) – эндотелиальный фактор роста; EMP (enzymes and metabolic pathways) – ферментные и метаболические процессы; MO – моноцит.
Под влиянием ИЛ-1, ИЛ-6 повышается концентрация эндотелиального фактора роста (VEGF). VEGF индуцирует ангиогенез, гиперплазию и пролиферацию интимы сосудов. Одновременно происходит изменение фенотипа B-клеток [7]. Оксидативный стресс, как патогенетический фактор, вызывает повреждение в средней оболочке артериальных сосудов, происходят быстрая гиперплазия и расширение интимы за счет изменения миофибробластов [20].
Клиническая картина
Ревматическая полимиалгия – заболевание суставов и периартикулярных структур – синовиальных сумок, сухожилий, энтезисов [21]. Заболевание чаще развивается остро. Симптоматика постепенно нарастает и через 26 недель достигает пика, при этом объективные изменения остаются незначительно выраженными. Возможно постепенное развитие со стертой клинической картиной, что значительно затрудняет своевременную диагностику [22]. Примерно в 50 % случаев первыми проявляются общие симптомы: снижение веса, слабость, субфебрильная температура, депрессия, потеря аппетита. У отдельных пациентов описаны, особенно после перенесенной вирусной инфекции, колебания АД [23]. Для полимиалгии характерно симметричное поражение. В дебюте заболевания возможно ассиметричное вовлечение суставов, но в течение нескольких дней поражение становится двусторонним [23].
Одним из основных клинических проявлений заболевания является выраженный болевой синдром в проксимальных группах мышц и параартикулярных мягких тканях плечевого и тазового пояса. Типичные жалобы: невозможность встать
с кровати или стула, собрать волосы без посторонней помощи. Частота вовлечения плечевого пояса по ризомиелическому типу составляет около 95 % случаев – боль и скованность в мышцах шеи с распространением на ключицы, верхнюю половину грудной клетки [22, 23]. Реже возникают дистальные симптомы, связанные с вовлечением запястий и пястно-фаланговых суставов, изменением коленных суставов. Стопы вовлекаются крайне редко. Примерно у 15 % больных развивается синдром запястного канала (туннельная нейропатия срединного нерва) [24]. Еще реже (до 10 %) встречается умеренно выраженный диффузный отек кистей со сгибательной контрактурой пальцев из-за ладонного фасцита и поражения сухожилий сгибателей пальцев, полностью купирующийся на фоне лечения ГКС. Субакромиальные/ субдельтовидные бурситы возникают у 96 % лиц с РПМА, специфичность этого признака составляет 99,1 % [26].
Миалгический синдром имеет ряд особенностей: боль постоянная, ноющего, тянущего характера, сохраняется в ночное время, усиливается при перемене положения тела. При пальпации определяется умеренная мышечная болезненность, которая не коррелирует со степенью миалгии, описываемой пациентом [22].
Двигательная скованность возникает в утренние часы после пробуждения, а также после длительного ограничения подвижности (феномен «геля»), обычно длится час и более. Скованность в области шеи и нижней части спины может быть связана с наличием межпозвонковых бурситов и энтезитов многочисленных связок позвоночника [24]. Обычные двигательные задания пациенты выполняют с трудом из-за вовлечения суставов и периартикулярных структур, сохраняя при этом нормальную мышечную силу. Объем движений в плечевых суставах, шейном отделе позвоночника, тазобедренных суставах ограничен без развития мышечных атрофий и гипотрофий [23, 24]. Характерным для РПМА является ограничение активных движений в плечевых суставах при сохранении пассивных. Пациент не может поднять руки на более чем 90 градусов, при этом не выявляются объективные клинические признаки суставного отека. Для описания основных проявлений ревматической полимиалгии была предложена аббревиатура SECRET [25]:
S – stiffness and pain – скованность и боли;
E – elderly individuals – пожилой возраст больных;
C – constitutional symptoms – общие конституциональные симптомы;
R – arthritis (rheumatism) – артрит;
E – elevated erythrocyte sedimentation rate (ESR) – повышенная COЭ;
T – temporal arteritis – височный артериит.
Диагностика
На сегодняшний день не существует единого клинического, лабораторного или инструментального признака, наличие которого позволило бы подтвердить диагноз РПМА. Диагностику проводят по совокупности проявлений болезни.
Современные классификационные критерии, разработанные экспертами Американской коллегии ревматологов и Европейской антиревматической лиги, наряду с клини-
ческими и лабораторными представлены в табл. 1 [26].
Облигатным признаком РПМА, встречающимся практически у каждого пациента в активной фазе заболевания, является значительное повышение скорости оседания эритроцитов (СОЭ) выше 30–40 мм/ч. Диагностически значимым повышением СРБ принято считать уровень более 6 мг/дл. Кроме того, наблюдается повышение других неспецифических показателей активности РПМА – уровня Среактивного белка (СРБ), фибриногена, альфа-2-глобулинов, интерлейкина-6. Как правило, снижается уровень гемоглобина, но не ниже 90 г/л, анемия носит нормохромный, нормоцитарный характер [22, 25, 27]. Миозитспецифические ферменты демонстрируют нормальные значения (креатинфосфокиназа, миоглобин, альдолаза). Ревматоидный фактор, антитела к циклическому цитруллированному пептиду.
Антинуклеарные антитела негативны.
Основными инструментальными методами диагностики РП являются УЗИ, МРТ и ПЭТ-КТ с 18-дезоксифтороглюкозой (18-ДФГ) суставов и околосуставных тканей. Для РПМА характерно наличие синовита плечевых суставов, теносиновитов бицепсов, субакромиальный и субдельтовидный бурсит; синовит тазобедренных суставов, подвздошно-поясничный бурсит и трохантерный бурсит; шейные и поясничные межпозвонковые бурситы периартикулярных тканей и височных артерий. КТ и МРТ показаны при атипичных симптомах (боль внизу спины или боль в ногах). При гистологическом исследовании синовиальной оболочки больных РПМА наблюдается слабо выраженная воспалительная инфильтрация с преобладанием макрофагов и CD4 Т-клеток [24, 25].
Таблица 1
Классификационные критерии ревматической полимиалгии EULAR/ACR (2015) [26]
| Обязательные критерии | ||
| ||
| Критерии | Подсчет при отсутствии данных УЗИ (0–6 баллов) | Подсчет при наличии данных УЗИ (0–8 баллов) |
| Утренняя скованность дольше 45 мин | 2 | 2 |
| Боль в тазобедренных суставах или ограничение их подвижности | 1 | 1 |
| Отсутствие РФ и АЦЦП | 2 | 2 |
| Отсутствие вовлечения других суставов | 1 | 1 |
| УЗ-критерии | ||
| По крайней мере одно плечо с субдельтовидным бурситом, и (или) тендовагинитом бицепса, и (или) синовитом плечевого сустава (задний или подмышечный), синовит по крайней мере одного тазобедренного сустава и (или) трохантерный бурсит | – | 1 |
| Оба плеча с поддельтовидным бурситом, тендовагинитом бицепса или синовитом плечевого сустава | – | 1 |
| Подтверждение диагноза РПМА | ||
| ≥ 4 баллов при отсутствии данных УЗИ ≥ 5 баллов при наличии данных УЗИ |
Дифференциальная диагностика
Дифференциальная диагностика ревматической полимиалгии крайне сложна. Для окончательной постановки диагноза необходим скрининг выявления других нозологий (табл. 2) [27]. Особенно тщательно она должна проводиться у пожилых пациентов с коморбидным анамнезом (АГ, ОНМК, головокружениями неясного генеза, болезнью Паркинсона) [28, 29].
Таблица 2
Дифференциальная диагностика ревматической полимиалгии [27]
| Воспалительные заболевания | |
| Заболевание | Отличительные признаки |
| Ревматоидный артрит, особенно пожилого возраста | Симметричный артрит, преимущественно дистальное вовлечение суставов. Лабораторно выявляются РФ+ (в пожилом возрасте может быть положительным при отсутствии заболевания), АЦЦП+. Рентгенологически выявляются эрозии суставных поверхностей костей. С течением времени присоединяются внесуставные проявления |
| Поздние спондилоартриты (возраст 50 лет и старше) | Типично воспалительное поражение позвоночника. Боль и скованность внизу спины, анкилоз позвонков или сакроилеит на рентгенограмме и МРТ, периферический моно- или несимметричный олигоартрит. Возможны энтезиты пяточных костей, дактилиты и передние увеиты. Ассоциация с антигеном HLA B 27 |
| RS 3PE-синдром (синдром подушкообразных кистей) | Симметричный дистальный синовит. Мягкий отек кистей или стоп, оставляющий ямочку при надавливании пальцем. Редко регистрируется как самостоятельное заболевание, чаще сочетается с РА (особенно РАПВ), а также РПМА |
| Воспалительная миопатия | Клинически прогрессирующая выраженная мышечная слабость проксимальных мышц, высыпания. Высокие концентрации креатинфосфокиназы, лактатдегидрогеназы. Характерные изменения при проведении игольчатой электромиографии |
| Микрокристаллическая артропатия (болезни депозитов пирофосфата кальция и гидроксиапатита) | Вовлекаются плечевые суставы, карпальные каналы, коленные суставы; выявляются рентгенологически и по ультрасонографии, кристаллы в синовиальной жидкости при поляризационной микроскопии. Основные клинические особенности: пожилой возраст установления диагноза, остеоартрит коленных суставов, кальцификация сухожилий и артрит голеностопного сустава |
| Другие заболевания соединительной ткани | Патологическая утомляемость, мультисистемность болезни, аутоантитела – характерные для конкретного заболевания (анти-дсДНК, снижение сывороточных концентраций C 3- и С4-компонентов комплемента) |
| Невоспалительные заболевания | |
| Адгезивный капсулит, синдром вращательной манжеты плеча | Одностороннее поражение, околосуставная (локальная) болезненность. Ограничение активных движений при полном сохранении пассивных. Лабораторно выявляются воспалительные изменения |
| Дегенеративные болезни суставов, остеоартрит | Механические боли в суставах, СОЭ и концентрация СРБ обычно нормальные. Рентгенологически выявляются дегенеративные изменения |
| Фибромиалгия | Генерализованные костно-мышечные боли с распространением на грудную клетку, позвоночник, дистальные отделы конечностей. Невыраженное ограничение движения в суставах, не приводящее к нарушению самообслуживания. Характерны нарушение сна, психологические особенности (депрессия, тревожные расстройства), а также утомляемость, продолжительная боль, множественные триггерные зоны |
| Инфекционные заболевания | |
| Вирусная и бактериальная инфекция (бактериальный эндокардит, микобактериальная инфекция) | Особенности истории болезни. Лихорадка, потеря массы тела, шум в сердце. Миалгии носят генерализованный характер, не вызывая существенных ограничений движения. Лабораторно – лейкоцитоз, изменения в анализах мочи, положительные серологические исследования крови на вирусы, посев крови |
| Злокачественные заболевания | |
| Солидные опухоли (почки, желудок, легкие, кишечник и др.) | Потеря массы тела, утомляемость, симптомы диффузной боли, не ограниченные плечевым или тазовым поясом. Зависимость оценки от симптомов, аномальные симптомы при физикальном исследовании. Возможно обнаружение новообразования при проведении инструментальной диагностики. Часто реакция со стороны периферических лимфоузлов. Лабораторно – повышение концентрации онкомаркеров |
| Миеломная болезнь | Потеря массы тела, утомляемость. Боль в области пораженных позвонков в пояснично-крестцовой области и грудной клетке, реже в длинных трубчатых костях. Патологические переломы, очаги деструкции или диффузного остеопороза на рентгенограммах. Лабораторно – гиперпротеинемия, гиперкальциемия, М-протеин |
| Другие заболевания | |
| Паркинсонизм | Постепенное начало; скованность, ригидность без болевого синдрома, шаркающая походка, тремор |
| Болезни щитовидной и паращитовидной желез | Типичные синдромы соответствующей эндокринопатии, повышенная или пониженная концентрация тиреотропного / парат-гормона, изменения со стороны кальций-фосфорного обмена, поведенческие особенности (депрессия, повышенная возбудимость) |
| Гиповитаминоз D | Нелокализованная миалгия, слабость преимущественно проксимальных отделов конечностей, склонность к падениям, вызванная остеомаляцией. Лабораторно – повышение активности щелочной фосфатазы, снижение концентрации кальция, витамина D в сыворотке |
| Лекарственно-индуцированная миопатия (статины, колхицин, глюкокортикостероиды) | Отсутствие системных симптомов, улучшение после отмены препарата, повышение мышечных ферментов (преимущественно креатинфосфокиназы), положительные антитела к 3-гидрокси-3-метилглютарилкофермент А редуктазе (анти HMG-CoA) |
| Стеноз позвоночного канала | Онемение, парестезии, мышечная слабость преимущественно нижних конечностей, нормальные уровни маркеров воспаления |
Терапия РПМА
Лечение пациентов с РПМ должен проводить врачревматолог с предварительной консультацией терапевта и невролога (для исключения дегенеративных заболеваний позвоночника). Для уменьшения болей, связанных с сопутствующим остеохондрозом, артритом, возможно применение НПВП, которые дают хороший симптоматический (анальгетический) эффект, но не оказывают влияния на воспалительный процесс, обусловленный РПМ, и прогноз заболевания, могут вызывать тяжелые неблагоприятные реакции со стороны желудочнокишечного тракта и сердечно-сосудистой системы [4, 30–33].
Основой лечения РПМА является пероральная терапия глюкокортикоидами (ГКС). Лечение подразделяется на несколько основных этапов: начальную терапию ГКС (индукцию ремиссии), поддерживающую терапию
(снижение суточной дозы) и период отмены ГКС [26]. Стратегия терапии ГКС представлена на рисунке 2 [32].
Рекомендуемая начальная доза преднизолона составляет 15 мг в день. Меньшие дозы (7,5–10,0 мг в день) могут быть рассмотрены для пациентов с меньшим ИМТ, более легкими симптомами, неконтролируемым диабетом или риском серьезных побочных эффектов лекарств. Пациентам с бóльшим индексом массы тела или тяжелыми симптомами следует рассмотреть дозы 20–25 мг в день. Быстрое улучшение симптомов при использовании низких доз преднизолона (менее 15 мг) считается достоверным диагностическим признаком РПМА. Однако этот ответ неспецифичен для ревматической полимиалгии, так как другие воспалительные артриты (например, ревматоидный артрит, остеоартрит, кристаллические артропатии) также могут позитивно реагировать на низкие дозы глюкокортикостероидов. Уровни СОЭ и СРБ обычно нормализуются в течение 2–4 недель после начала лечения, что коррелирует с улучшением клинической картины. Дозу глюкокортикоидов, контролирующую симптомы, обычно поддерживают в течение 2–4 недель после исчезновения боли и скованности. Затем дозу снижают каждые 2–4 недели по переносимости до минимальной поддерживающей дозы. Снижение дозы 10 мг следует замедлить до 1 мг каждые 1–2 месяца. Типичное лечение длится 1–2 года. Снижение дозы стероидов до исчезновения симптомов или слишком быстро после исчезновения симптомов может привести к более высокому уровню рецидивов и снижению вероятности стойкой ремиссии после прекращения лечения. [2, 31]. Если в течение 1–2 недель после начала терапии нет клинико-лабораторного ответа, следует повысить уровень преднизолона или рассматривать альтернативные диагнозы. При повторном подтверждении РПМА следует рассматривать парентеральное введение или прием ГКС два раза в день. Разделять дозу препарата на несколько приемов следует в случае выраженного интенсивного болевого синдрома в ночное время суток.
К альтернативным вариантам лечения относится стероидосберегающая терапия. Возможно раннее назначения метотрексата (МТ) в дополнение к терапии ГКС, особенно у больных с высоким риском рецидива, а также у лиц с коморбидной патологией, у пациентов, находящихся в ремиссии, но не даю-
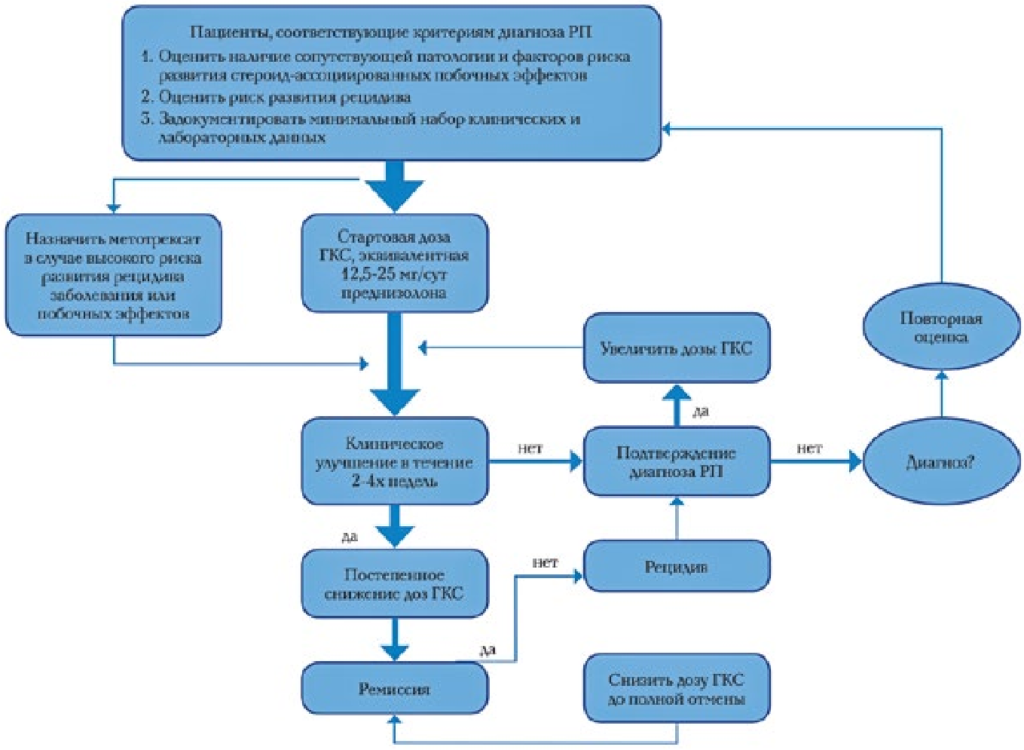
Рисунок 2. Алгоритм лечения ревматической полимиалгии согласно рекомендациям EULAR/
ACR 2015 [32]
щих желаемого ответа на терапию ГКС. Целью использования метотрексата является уменьшение продолжительности приема и кумулятивной дозы ГК, а также снижение риска нежелательных реакций, обусловленных приемом последних. Рекомендуемая доза МТ составляет 7,5–10,0 мг в неделю для перорального приема [2, 31]. Другие препараты иммуносупрессивного действия (например, азатиоприн) и ингибиторы фактора некроза опухоли альфа не показали своей эффективности.
ИЛ-6 играет важную роль в поддержании активности болезни при РПМА, поэтому блокаторы ИЛ-6 были изучена в качестве альтернативного лечения с многообещающими результатами. В последние годы продемонстрирована эффективность тоцилизумаба (ТЦЗ) при РПМ и ГКА [2, 32]. Показаниями для назначения ТЦЗ (стандартной дозы 8 мг/кг в месяц) были резистентность к ГК (необходимость приема высокой дозы для поддержания ремиссии) или сопутствующие заболевания, которые ограничивали возможность адекватной терапии ГК. В исследованиях в течение 1–3 месяцев терапии был выраженный клинико-лабораторный эффект, позволяющий уменьшить дозу ГК. Имеются также данные о сохранении ремиссии после отмены ТЦЗ [18, 27]. Тем не менее плохо изучены риски длительного применения ТЦЗ, включая возможное увеличение риска инфекций и сердечно-сосудистых осложнений, поэтому сформулированы четкие показания к назначению тоцилизумаба [2]:
- как препарата первой линии в комбинации с ГКС у пациентов с тяжелыми сопутствующими заболеваниями для быстрого снижения дозы стероидов;
- как препарата второй линии у пациентов, которые нуждаются в комбинированной терапии, для достижения стероидосберегающего эффекта, а также при рефрактерности к метотрексату, плохой переносимости этого препарата или высоком риске развития нежелательных реакций;
- в качестве препарата второй линии при частом рецидивировании иммуновоспалительного процесса на фоне снижения дозы ГКС [2, 31, 32].
Заключение
РПМ – заболевание, не имеющее специфических диагностических маркеров, что значительно затрудняет дифференциальную диагностику и своевременную терапию. Дальнейшее изучение этиологических факторов, особенно генетических, использование методов фармакогенетики заболевания позволит своевременно выявлять и проводить специфическую терапию данного заболевания.
Список литературы / References
- González-Gay MA, Matteson EL, Castañeda S. Polymyalgia rheumatica. Lancet 2017; 390: 1700–12.
- В. Н. Коваленко, И. Ю. Головач, О. П. Борткевич, Практические акценты диагностики и лечения ревматической полимиалгии; 27.12.2019. Тематичний номер «Кардіологія, Ревматологія, Кардіохірургія» № 5 (66), 2019. Интернет-портал https://www.health—ua. com/article/45290-prakticheskie—aktcenty—diagnostiki—ilecheniya—revmaticheskoj—polimialgii
- Kovalenko, I. Yu. Golovach, O. P. Bortkiewicz. Practical accents in the diagnosis and treatment of polymyalgia rheumatica. 12/27/2019. Thematic issue ‘Cardiology, Rheumatology, Cardiosurgery’ No. 5 (66), 2019. Internet portal https://www.health-ua.com/ article/45290-prakticheskie-aktcenty-diagnostiki-ilecheniya-revmaticheskoj-polimialgii
- González-Gay MA, Vazquez-Rodriguez TR, Lopez-Diaz MJ, et al. Epidemiology of giant cell arteritis and polymyalgia rheumatica. Arthritis Rheum. 2009; 61: 1454–61.
- Путилина М. В., Солдатов М. А. Церебральные инсульты в старческом возрасте. Особенности клинической картины, течение, лечение. Врач. 2006; 5: 29–34.
Putilina M. V., Soldatov M. A. Cerebral strokes in old age. Features of the clinical picture, course, treatment. Doctor. 2006; 5: 29–34.
- Ughi N., Sebastiani G., Gerli R., Salvarani C., Parisi S., Ariani A., Prevete I., Manara M., Rumi F., Sciré C., & Bortoluzzi A. (2020). The Italian Society of Rheumatology clinical practice guidelines for the management of polymyalgia rheumatica. Reumatismo, 72 (1), 1–15. https://doi.org/10.4081/reumatismo.2020.1268.
- Salvarani C, Cantini F, Hunder GG. Polymyalgia rheumatica and giant-cell arteritis. Lancet. 2008; 372 (9634): 234–45. DOI: 10.1016/S 0140–6736(08)61077–6.
- Дорохов Г. Ю., Гордиенко А. В., Маковеева О. В., Барсуков А. В. Ревматическая полимиалгия: особенности клинической картины и диагностики. Вест. рос. военно-медицинской академии; 2017, 2 (58): 213–217.
Dorokhov G. Yu., Gordienko A. V., Makoveeva O. V., Barsukov A. V. Polymyalgia rheumatica: features of the clinical picture and diagnosis; West. grew up military medical academy; 2017. 2 (58): 213–217.
- Guggino G., Ferrante A., Macaluso F., Triolo G., Ciccia F. Pathogenesis of polymyalgia rheumatica. Reumatismo. 2018; 70 (1): 10–17. Published 2018 Mar 27. DOI: 10.4081/ reumatismo.2018.1048.
- Elling Р., Olsson A. T., Elling H. Synchronous variations in the incidence of temporal arteritis and polymyalgia rheumatica in Danish countries. Association with epidemics of Mycoplasma pneumonia infection. Ugeskrift Laeger. 1997; 159: 4123–8.
- Drago F., Ciccarese G., Agnoletti A. F., et al. Remitting seronegative symmetrical synovitis with pitting edema associated with parvovirus B 19 infection: two new cases and review of the comorbidities. Int J Dermatol. 2015; 54: 389–93.
- Cimmino M. A., Caporali R., Montecucco C. M., et al. A seasonal pattern in the onset of polymyalgia rheumatica. Annals Rheum Dis. 1990; 49: 521–3.
- Kampstra A. S.B., Toes R. E.M. HLA class II and rheumatoid arthritis: the bumpy road of revelation. Immunogenetics. 2017; 69 (8–9): 597–603. DOI: 10.1007/s00251–017–0987–5.
- Salvarani C., Cantini F., Olivieri I. Distal musculoskeletal manifestations in polymyalgia rheumatica. Clin Exp Rheumatol. 2000; 18 (4 Suppl 20): S 51–S 52.
- Gonzalez-Gay M.A., Garcia-Porrua C., Salvarani C., et al. Polymyalgia manifestations in different conditions mimicking polymyalgia rheumatica. Clin Exper Rheumatol. 2000; 18: 755–9.
- Путилина М. В. Роль дисфункции эндотелия при цереброваскулярных заболеваниях Врач; 2012, 7: 24–28.
Putilina M. V. The role of endothelial dysfunction in cerebrovascular diseases. Doctor; 2012, 7: 24–28.
- Dejaco C., Duftner C., Buttgereit F., et al. The spectrum of giant cell arteritis and polymyalgia rheumatica: revisiting the concept of the disease. Rheumatology. 2017; 56: 506–15.
- Dejaco C, Duftner C, Al-Massad J, et al. NK-G2D stimulated T-cell autoreactivity in giant cell arteritis and polymyalgia rheumatica. Annals Rheum Dis. 2013; 72: 1852–9.
- Buttgereit F., Dejaco C., Matteson E. L., Dasqupta B. Polymyalgia Rheumatica and Giant Cell Arteritis: A Systematic Review; JAMA; 2016, V. 315 (22): 2442–2458.
- Lee GH, Lee WW. Unusual CD 4+CD 28– T Cells and Their Pathogenic Role in Chronic Inflammatory Disorders. Immune Netw. 2016; 16 (6): 322–329. DOI: 10.4110/in.2016.16.6. 322doi:10.1186/ar3140.
- Коваленко В. М., Борткевич О. П., Головач И. Ю. Практические акценты диагностики и лечения ревматической полимиалгии. Здоров’я України. Кардіологія, ревматологія, кардіохірургія; 2019, 5 (66): 25–27.
- Kovalenko, O. P. Bortkevich, and I. Yu. Golovach. Practical accents in the diagnosis and treatment of polymyalgia rheumatica. Health of Ukraine. Cardiology, rheumatology, cardiosurgery; 2019, 5 (66): 25–27.
- Mahmood S. B., Nelson E., Padniewski J., & Nasr R. (2020). Polymyalgia rheumatica: An updated review. Cleveland Clinic Journal of Medicine, 87 (9), 549–556.
- Башкова И. Б., Тарасова Л. В., Бусалаева Е. И. Ревматическая полимиалгия. Медицинский альманах; 2018, 1 (52): 142–146.
Bashkova I. B., Tarasova L. V., Busalaeva E. I. Polymyalgia rheumatica. Medical Almanac; 2018, 1 (52): 142–146.
- Теплова Н. В., Евсиков Е. М. Блокатор ангиотензиновых рецепторов Валсартан (Диован) в клинической практике. РМЖ. 2005; 14: 944.
Teplova N. V., Evsikov E. M. Angiotensin receptor blocker Valsartan (Diovan) in clinical practice. RMJ. 2005; 14: 944.
- Сатыбалдыев А. М., Демидова Н. В., Савушкина Н. М., Гордеев А. В. Ревматическая полимиалгия. Научно-практическая ревматология; 2018, 56 (2): 215–227.
Satybaldyev A. M., Demidova N. V., Savushkina N. M., Gordeev A. V. Polymyalgia rheumatica. Scientific and Practical Rheumatology; 2018. 56 (2): 215–227.
- Сатыбалдыев А. М. Эволюция диагностики ревматической полимиалгии. Научнопрактическая ревматология. 2019; 57 (6): 693–698.
Satybaldyev A. M. Evolution of the diagnosis of polymyalgia rheumatica. Scientific and Practical Rheumatology. 2019; 57 (6): 693–698.
- Головач И. Ю. Основные принципы новых диагностических критериев (2012) и рекомендаций ACR/EULAR’2015 по менеджменту и лечению ревматической полимиалгии. Український ревматологічний журнал; 2016, 2 (64): 3–7.
Golovach I. Yu. Basic principles of the new diagnostic criteria (2012) and ACR/EULAR’2015 guidelines for the management and treatment of polymyalgia rheumatica. Ukrainian Rheumatological Journal; 2016. 2 (64): 3–7.
- Башкова И. Б., Бусалаева Е. И. Ревматическая полимиалгия: редко диагностируемое, но нередко встречающееся заболевание. РМЖ. Медицинское обозрение.
2017; 25 (1): 48–52.
Bashkova I. B., Busalaeva E. I. Polymyalgia rheumatica: a rarely diagnosed but common disease. breast cancer. RMJ. Medical review. 2017; 25 (1): 48–52.
- Теплова Н. В., Люсов В. Н., Оганов Р. Г., Евсиков Е. М., Шарипов Р. А. Нефрогенные факторы формирования резистентности к антигипертензивной терапии у больных первичной артериальной гипертензией; Рациональная фармакотерапия в кардиологии. 2015; 6 (11): 590–594.
Teplova N. V., Lyusov V. N., Oganov R. G., Evsikov E. M., Sharipov R. A. Nephrogenic factors of resistance formation to antihypertensive therapy in patients with primary arterial hypertension; Rational Pharmacotherapy in Cardiology. 2015; 6 (11): 590–594.
- Путилина М. В., Баранова О. А. Результаты многоцентровой клинико-эпидемиологической наблюдательной программы «ГЛОБУС» (определение распространенности головокружения и оценка схем терапии на амбулаторном уровне). Журнал неврологии и психиатрии им. С. С. Корсакова. 2014; 114 (5): 33–38. Putilina M. V., Baranova O. A. Results of the multicenter clinical and epidemiological observational program GLOBUS (determination of the prevalence of dizziness and assessment of therapy regimens at the outpatient level). Journal of Neurology and Psychiatry n. a. S. S. Korsakov. 2014; 114 (5): 33–38.
- Путилина М. В., Теплова Н. В. Лекарственная безопасность как приоритетное направление отечественной медицины. Лечебное дело. 2019; 4: 7–14. DOI:
10.24411/2071–5315–201912152.
Putilina MV, Teplova NV. Medicinal safety as a priority area of domestic medicine. General Medicine. 2019; 4: 7–14. DOI: 10.24411/2071–5315–2019–12152.
- Vatutin N. T., Smirnova A. S., Taradin G. G., ElKhatib M. A. Review of guidelines for the treatment of polymyalgia rheumatica (EULAR/ACR 2015). Archive of internal medicine. 2016; 6 (1): 3–5.
- Dejaco C., Singh Y. P., Perel P., et al. 2015 recommendations for the management of polymyalgia rheumatica: a European League Against Rheumatism / American College of Rheumatology collaborative initiative. Arthritis Rheumatol. 2015; 67 (10): 2569–2580. DOI: 10.1002/art.39333.
- Путилина М. В., Теплова Н. В., Громова О. А., Торшин И. Ю., Максимова М. Ю., Прокофьева Ю. С. Двигательные расстройства у пациентов пожилого возраста c хроническими заболеваниями опорно-двигательного аппарата (локомотивным синдромом). Неврология, нейропсихиатрия, психосоматика. 2021; 13 (2): 130–136. DOI: 10.14412/2074–2711–2021–2–130–136.
Putilina M. V., Teplova N. V., Gromova O. A., Torshin I. Yu., Maksimova M. Yu., Prokofieva
Yu. S. Neurology, neuropsychiatry, psychosomatics. Motor dysfunction in elderly patients with chronic musculo-skeletal system diseases (locomotive syndrome) 2021; 13 (2): 130–136. DOI: 10.14412/2074–2711–2021–2–130–136.
Сведения об авторах
Теплова Наталья Вадимовна, д. м. н., проф., зав. кафедрой клинической фармакологии лечебного факультета1. E—mail: teplova.nv@yandex.ru. ORCID: 0000–0002–7181–4680
Путилина Марина Викторовна, д. м. н., проф., проф. кафедры клинической фармакологии лечебного факультета1. E—mail: profput@mail.ru. ORCID: 0000–0002–8655–8501
Червякова Галина Александровна, к. м. н., доцент кафедры клинической фармакологии лечебного факультета1. ORCID: 0000–0002–6201–9669
Апокина Валерия Витальевна, ординатор кафедры клинической фармакологии лечебного факультета1
Никифорова Алина Викторовна, ординатор кафедры ревматологии2
1ФГАОУ ВО «Российский национальный исследовательский медицинский университет имени Н. И. Пирогова» Минздрава России, Москва
2ФГБНУ «Научно-исследовательский институт ревматологии имени В. А. Насоновой», Москва
Автор для переписки: Теплова Наталья Вадимовна. E-mail: teplova.nv@yandex.ru
About authors
Teplova Natalya V., DM Sci (habil.), professor, head of Dept of Clinical Pharmacology, Faculty of Medicine1. E-mail: teplova.nv@yandex.ru. ORCID: 0000–0002–7181–4680
Putilina Marina V., DM Sci (habil.), professor, professor at Dept of Clinical Pharmacology, Faculty of Medicine1. E-mail: profput@mail.ru. ORCID: 0000–0002–8655–8501
Chervyakova Galina A., PhD Med, associate professor at Dept of Clinical Pharmacology, Faculty of Medicine1. ORCID: 0000–0002–6201–9669
Apokina Valeria V., intern of Dept of Clinical Pharmacology, Faculty of Medicine1
Nikiforova Alina V., resident of Dept of Rheumatology2
1Pirogov Russian National Research Medical University, Moscow, Russia
2V. A. Nasonova Research Institute of Rheumatology, Moscow, Russia
Для цитирования: Теплова Н. В., Путилина М. В., Червякова Г. А., Апокина В. В., Никифорова А. В. Сложности дифференциальной диагностики и современные подходы к терапии ревматической полимиалгии. Медицинский алфавит. 2022; (1): 29–34. https://doi.org/10.33667/2078-5631-2022-1-29-34 | For citation: Teplova N. V., Putilina M. V., Chervyakova G. A., Apokina V. V., Nikiforova A. V. Diffculties in differential diagnosis and modern approaches to treatment of polymyalgia rheumatica. Medical alphabet. 2022; (1): 29–34. https://doi. org/10.33667/2078-5631-2022-1-29-34 |
Corresponding author: Teplova Natalya V. E-mail: teplova.nv@yandex.ru

